Врачи-радиологи из Центра здоровья мозга Университета Техаса в Далласе предложили на страницах журнала Journal of Neuroimaging способ, который поможет усовершенствовать диагностику рассеянного склероза.
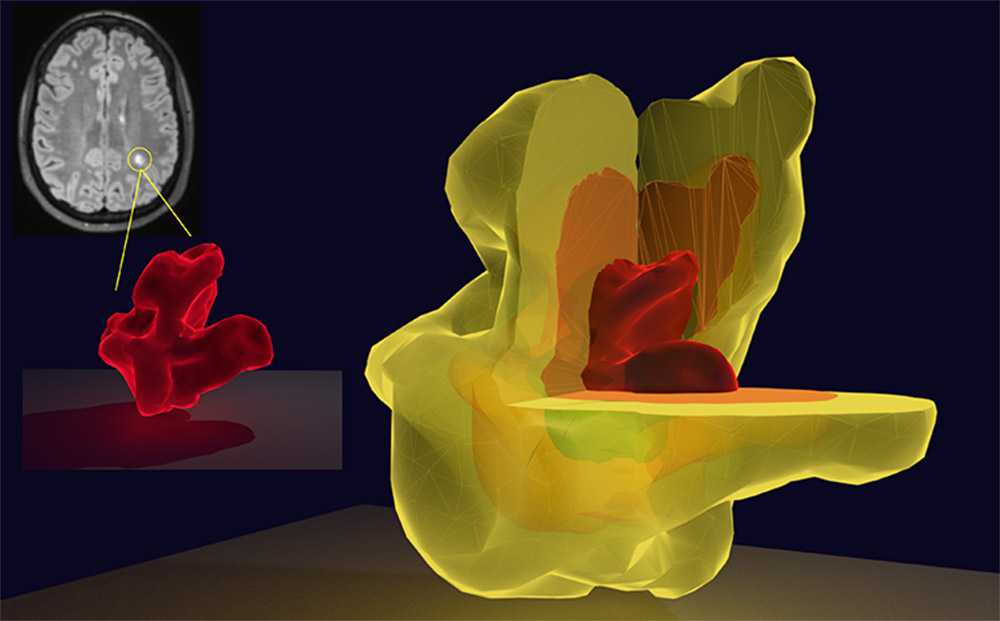
На основании данных о метаболической и функциональной активности очагов патологии в мозге они визуализировали их в 3D и определили, что по форме получившихся моделей можно предугадывать потенциал ремиелинизации или дальнейшего прогрессирования.
Рассеянный склероз – это заболевание аутоиммунной природы, которое проявляется разрушением миелинового слоя вокруг отростков нейронов, что значительно ухудшает передачу нервного импульса между клетками. Диагноз ставится совместно как неврологами, так и врачами лучевой диагностики на основании клинической картины и специфических МРТ-признаков, описанных критериями Макдональда.
Для этого используются стандартные 2Dсканы МРТ. Согласно критериям, есть признаки прогрессирования болезни (диссеминации) в пространстве, когда очаги обнаруживаются в определенных уязвимых местах мозга, и во времени, когда их количество увеличивается при следующей МРТ. Однако, предусмотреть, какие очаги «остановятся» в росте или даже «уменьшатся» (из-за ремиелинизации), а какие – продолжат расти, невозможно. Соответственно, динамику и ответ на лечение предугадать затруднительно.
Американские исследователи предложили использовать для этой цели вычислительный инструмент, который позволяет сконструировать 3Dмодель очага рассеянного склероза на основе его физиологических характеристик. Как выяснилось, форма и текстура поверхности получаемой модели хорошо коррелирует с метаболической активностью очага и позволяет прогнозировать его развитие или регресс.
Для работы радиологи использовали 109 снимков в последовательностях T2-FLAIR и фМРТ, полученные на томографах с напряженностью магнитного поля 3 Тесла от 23 человек. На T2-FLAIR с тонкими срезами они выделяли очаг во всех трех проекциях. Калибровка фМРТ – типа МРТ, улавливающего изменения в использовании кислорода «молчащими» и активными нейронами (сигнал BOLD) – позволила им измерить собственно BOLD, уровень церебрального кровотока (CBF) и скорость метаболизма кислорода в мозге (CMRO2), то есть все метаболические характеристики конкретного очага. Целостность же белого вещества (нервных волокон) измеряли с помощью диффузионно-куртозисных изображений.
Сигнал BOLD изменялся от центра очага к периметру, то есть имел определенный «уклон», который, как выяснилось, хорошо «описывал» метаболические качества патологического места. Положительный уклон сочетался с высоким CMRO2и CBF и говорил об активности очага, тогда как отрицательный уклон BOLD коррелировал с низкими значениями CMRO2и CBF, что говорило о неактивном процессе.
Исследователи выяснили, что это хорошо описывается формой получавшейся 3Dконтрукции. Метаболически активные повреждения с большей целостностью белого вещества имели более симметричную форму и более сложную, изрезанную текстуру поверхности по сравнению с неактивными повреждениями, у которых форма была менее правильной, но с более ровными краями.
Авторы работы считают, что этот метод поможет более точно предсказывать дальнейшее развитие патологии и эффект от лечения, а значит, станет прекрасным помощником как для клиницистов, так и для врачей лучевой диагностики.
Текст: Анна Хоружая