Помимо сложных и зачастую достаточно инвазивных методов диагностики разных стадий болезни Альцгеймера исследователи активно «щупают» возможности неинвазивных рутинных методик.
Но если простая структурная магнитно-резонансная томография не обладает высокой специфичностью, то дополнение ее алгоритмами машинного обучения может дать гораздо более точный результат. Таковой получили исследователи из Великобритании, добившись 98-процентной точности диагностики болезни Альцгеймера благодаря машинной обработке снимков мозга. Свои результаты они опубликовали в журнале Communications Medicine.
На сегодняшний день в диагностике болезни Альцгеймера (БА) нет методов, которые бы позволяли в ходе скрининга выявлять заболевание с высокой точностью до появления первых клинических признаков, не используя при этом высокотехнологичные и дорогостоящие методы. Национальный институт старения США и Ассоциация болезни Альцгеймера в 2020 году предложили классификационную систему ATN, включающую в себя сочетания различных биомаркеров, которые с достаточно высокой вероятностью могут говорить о наличии патологии. Под буквой «А» зашифрован бета-амилоид, обнаруживаемый в анализе цереброспинальной жидкости (ЦСЖ) или на позитронно-эмиссионной томографии мозга (ПЭТ), буква «Т» сообщает о наличии гиперфосфорилированного тау-белка (тоже в ЦСЖ или на ПЭТ), а «N» обозначает нейродегенерацию, выявляемую на МРТ или ПЭТ по увеличению объема ЦСЖ. Восемь возможных комбинаций этих биомаркеров говорят о разных вероятностях наличия у пациента БА.
В статьях последних лет (например, вот и вот) все чаще сообщается и о том, что одну из ключевых ролей в разрастании патологических бляшек и проявлении болезни играет активированная микроглия, вызывающая нейровоспаление. Тем более что активацию ее и астроцитов уже научились «видеть» на МРТ. Поэтому, скорее всего, скоро нужно будет добавлять в классификацию ATN еще и нейровоспалительные биомаркеры.
Но основная проблема всех этих анализов на биомаркеры заключается в их сложности и не всегда возможном масштабировании с сохранением высокого качества в каждой партии и каждой лаборатории. Кроме того, цереброспинальную пункцию, которая дает возможность получить ЦСЖ, нельзя назвать рутинным методом, доступным в каждом медицинском учреждении. А анализы на биомаркеры в крови пока что получаются слишком дорогими, когда дело переходит от науки к промышленной разработке и коммерческому распространению.
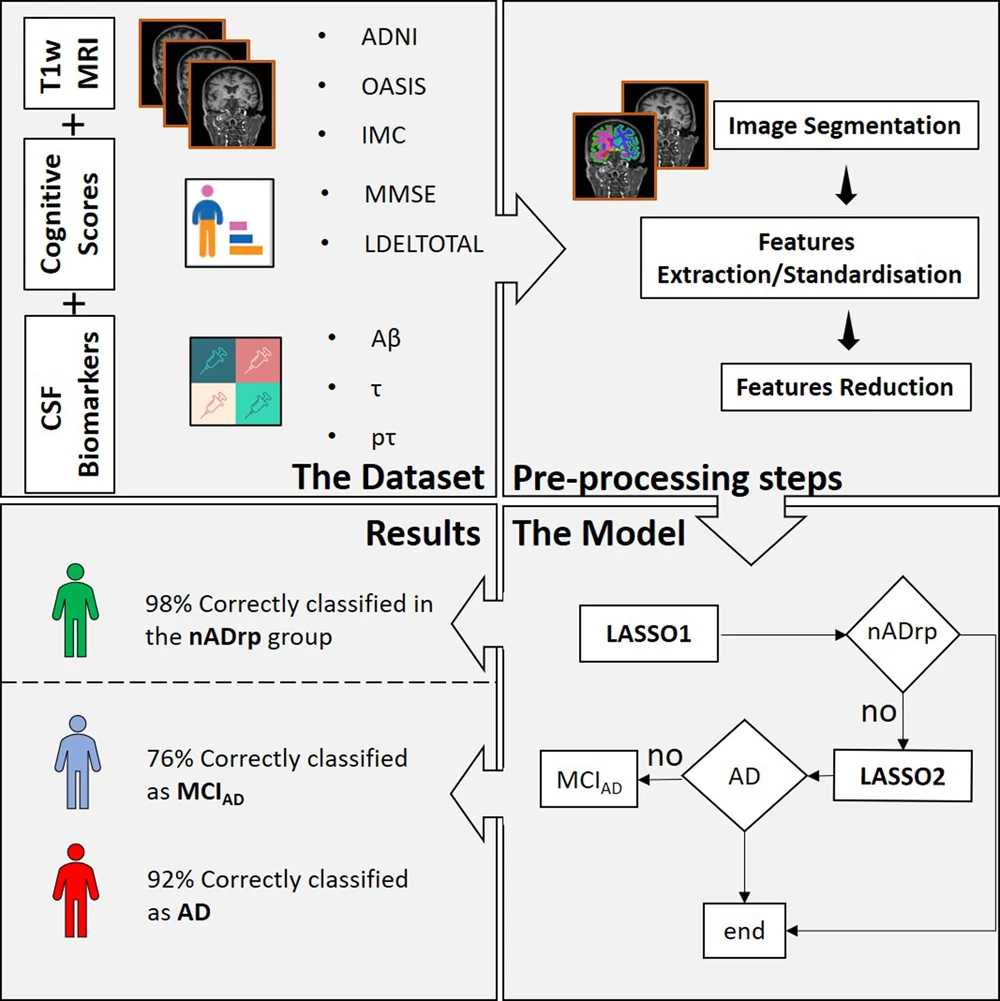
По этой причине с точки зрения массового скрининга населения самым подходящим методом кажется именно стандартная структурная МРТ. Здесь самым «ярким» признаком БА считается уменьшение объемов гиппокампа. Но есть проблема – этот признак не самый специфичный. То есть он вполне может встречаться и при других болезнях (шизофрения, депрессия или склероз гиппокампа). С другой стороны, БА может и не затрагивать гиппокампы – такие ее варианты тоже существуют. То есть нужен более глубокий структурный анализ, чтобы на снимках МРТ «заподозрить» неладное.
Такой анализ могут проводить алгоритмы машинного обучения, направленные на анализ невидимых глазу человека структурных изменений на МРТ в определенных областях интереса (наиболее подверженных патологическим изменениям). Этот подход заключается в сборе данных (для этого используется Т1-взвешенная последовательность с высоким разрешением MP-RAGE), их сегментации (деление на области), извлечении из сегментированных областей разных признаков (формы, текстуры, интенсивности, матрицы совпадения уровней серого (GLCM) и многих других), а затем статистической обработки этих признаков для выявления их связи с различными клиническими симптомами. Этот подход называется радиомикой, а признаки – радиомаркерами. И он оказался весьма перспективным в обнаружении признаков БА, например, по гиппокампу.
Чтобы разработать свой алгоритм, авторы новой статьи разделили мозг на 115 областей и выделили 660 различных признаков для оценки каждой области. Используя данные Инициативы по нейровизуализации болезни Альцгеймера (ADNI), где имелись не только МРТ снимки, но и клиническая информация о когнитивных функциях пациентов, они обучили алгоритм определять, какие из признаков могут точно предсказывать болезнь Альцгеймера. Далее команда протестировала свой алгоритм на МРТ мозга более чем 400 человек с ранней и поздней стадиями БА, а также здоровых людей и пациентов с другими неврологическими заболеваниями (включая лобно-височную деменцию и болезнь Паркинсона), входящих в контрольную группу.
Радиомаркеры, оказавшиеся «полезными» с точки зрения прогнозирования болезни, авторы статистическими методами объединили в общий, назвав его «прогностическим вектором болезни Альцгеймера» (ApV). Его рассчитали индивидуально для каждого пациента.
В итоге получилось, что алгоритм машинного обучения по МРТ научился определять, есть ли у человека БА, с 98-процентной точностью. Этот показатель значительно превосходит стандартные измерения объема гиппокампа и бета-амилоида в ЦСЖ. Он также с 79-процентной точностью оказался способен различать раннюю и позднюю стадию БА, чего ранее достичь не удавалось, в том числе и с помощью других моделей.
Кроме того, он выявил несколько интересных особенностей распространения патологии. В частности, он подтвердил, что биологические изменения тканей мозга затрагивают гиппокамп, энторинальную кору и миндалевидное тело, причем, на ранних стадиях преобладает значительное смещение дисфункций в левое полушарие (латерализация), подтверждая сильную латерализацию левого полушария (причем, это было обнаружено еще в ХХ веке). На поздних стадиях этого не наблюдалось.
Также алгоритм указал на области, которые ранее не считались связанными с БА: на мозжечок и вентральную часть промежуточного мозга (где в том числе расположен гипоталамус). Авторы считают, что этот результат бросает вызов традиционному мнению о том, что пучки белого вещества в мозжечке или в вентральном промежуточном мозге не подвержены влиянию БА. И, возможно, это подчеркнет новые терапевтические пути.
Исследователи отмечают, что их инструмент, который они проверили в том числе на внешнем наборе данных МРТ снимков (там он показал 86-процентную точность, что тоже весьма высоко) оказался «надежным и воспроизводимым при МРТ-сканировании, демонстрируя потенциал для применения в клинической практике в будущем».
Текст: Анна Хоружая