Центральное место в развитии понимания того, как работают нейронные сети, занимает разработка инвазивных мультимодальных интерфейсов, способных одновременно и записывать, и модулировать, то есть запускать активность нейронов непосредственно в головном мозге.
Главной проблемой этой технологии остается недолговечность инвазивных элементов из-за иммунного ответа со стороны окружающих тканей. Ученые из США разработали новый тип мультимодального микроэлектродного зонда, отличающийся крошечными размерами, гибкостью и большей безопасностью для окружающих тканей по сравнению с аналогами. Подробное описание разработки опубликовано в Nature Communications.
Микроэлектроды – важный инструмент в клинической и экспериментальной практике. Регистрация биопотенциалов с их помощью считается золотым стандартом измерения активности единичных нейронов с высоким временным разрешением в любой области нервной системы. Кроме того, локальная нейростимуляция, также осуществляемая при помощи микроэлектродов, позволяет определять роли нейронных цепей в управлении поведением.
Существующие ныне микроэлектродные массивы (матрицы) имеют важный недостаток: их большой размер и жесткость приводят к повреждению тканей и воспалению, что препятствует ведению долгосрочных записей электрических потенциалов в головном мозге. В качестве альтернативы предлагается, например, активно развивающийся метод оптогенетики. И хотя этот способ обеспечивает быструю активацию клеток, оптогенетическое взаимодействие с глубокими нейронными цепями из-за сильного рассеяния света и высоких поглощающих свойств нервной ткани требует имплантации жестких волокон большого диаметра. А это делает подход более инвазивным, чем его электрический аналог.
Разработать микроэлектродный зонд, лишенный недостатков предшественников, удалось ученым из Университета Калифорнии и Института биологических исследований Солка. Крошечный зонд гибкий и чрезвычайно тонкий — около одной пятой ширины человеческого волоса. Зонд способен регистрировать электрическую активность нейронов и стимулировать определенные участки с помощью света.
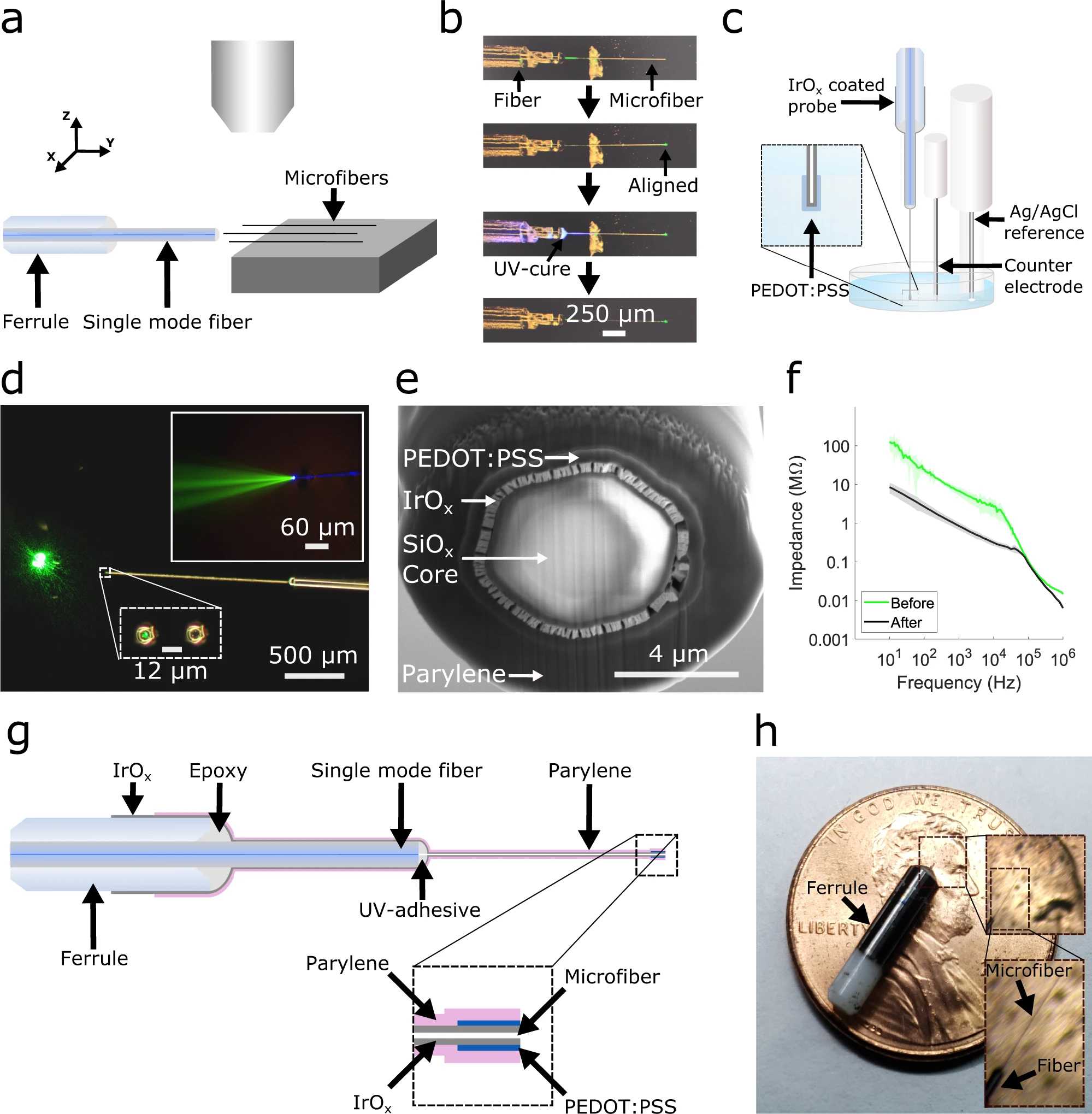
Состоит зонд из электрического канала с ультратонким полимерным электродом и оптического канала с таким же ультратонким оптическим волокном. Требования к изоляции двух каналов удалось выполнить за счет правильной комбинации материалов и оптимизированного изготовления электрического канала. Разработчики утверждают, что зонд идеально подойдет для изучения небольших областей нервной системы, таких как периферические нервы или спинной мозг. Зонд с легкостью сможет поместиться между позвонками для взаимодействия с нейронами и изгибаться при движении. Кроме того, эти свойства обеспечивают большую совместимость зонда с биологическими тканями и делает их менее склонными к запуску иммунного ответа, что, в свою очередь, может увеличить длительность использования.
Зонды диаметром всего от 8 до 14 микрометоров имплантировали в головной мозг живых мышей на срок до одного месяца. Когда мыши перемещались в контролируемой среде, зонды с высокой чувствительностью регистрировали электрическую активность нейронов. Также при нацеливании оптических каналов на определенные нейроны коры головного мозга (barrel cortex) удалось вызвать специфические физические реакции – движение усами. Важно отметить также и то, что зонды после длительного пребывания в ткани головного мозга вызывали более слабую иммунную реакцию по сравнению со стандартными мультимодальными волокнами.
Технология, по мнению создателей, станет востребованной в качестве минимально инвазивных интерфейсов для различных областей нервной системы. В дальнейшем ученые планируют провести эксперименты по внедрению зонда в спинной мозг: авторы работы считают, что созданная ими технология обладает уникальным потенциалом для изучения его на фундаментальном уровне и, более того, для получения способности модулировать его активность.
Учитывая то, что зонды вызывают лишь незначительную воспалительную реакцию, они предположительно дадут начало внедрению нового поколения легко настраиваемых мультимодальных устройств для долгосрочного и минимально инвазивного взаимодействия с нейронными цепями.
Текст: Анна Удоратина