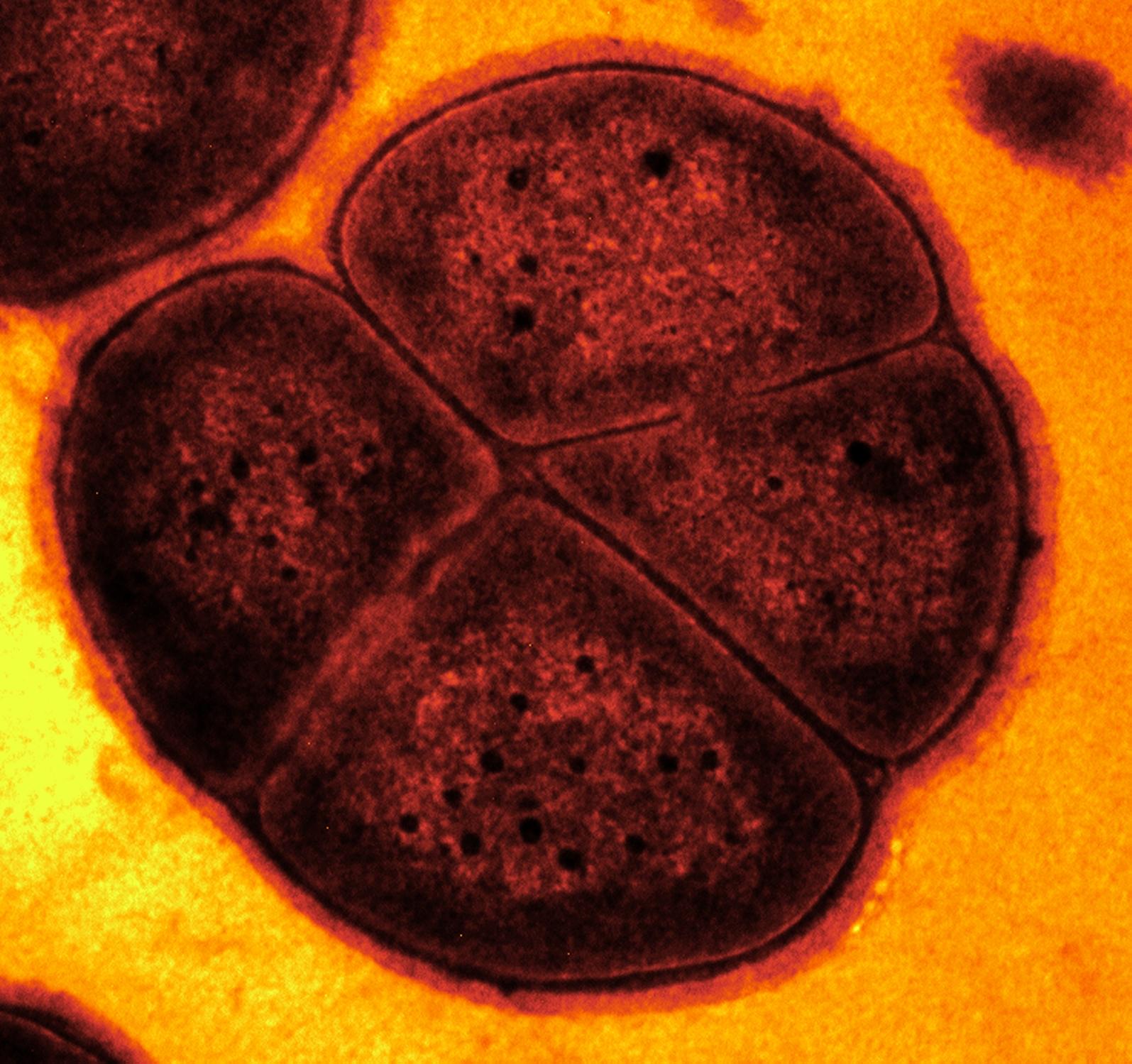
Как легендарная бактерия Deinococcus radiodurans ухитряется выживать в радиации, как излучение влияет на живые клетки и можно ли силу бактерий обратить против них самих, выяснили российские ученые.
Многие наслышаны о микроскопических беспозвоночных тихоходках (близкий к членистоногим тип Tardigrada), внешне напоминающих нечто среднее между надувным матрасом и плюшевым мишкой, которые и в воде не тонут, и космического излучения не боятся, и после криозаморозки оживают. Deinococcus radiodurans — «тихоходки» среди бактерий.
Хотя одноклеточные дейнококки сильно отличаются от своего эукариотического (имеющего ядра в клетках) многоклеточного собрата, они вовсе не уступают ему в живучести и могут выдерживать дозу радиации до 10 тыс. Грей (для человека доза 5 Грей смертельна), высушивание и химическое воздействие.
«О молекулярных механизмах регуляции экспрессии генов у этой бактерии известно относительно мало, — рассказывает Андрей Кульбачинский, профессор РАН, заведующий лабораторией в Институте молекулярной генетики РАН. — Мы исследовали уникальные белки этой бактерии, которые регулируют активность РНК-полимеразы — главного фермента, ответственного за считывание генетической информации с матрицы ДНК. Было показано, что эти белки (Gfh-факторы) способны останавливать РНК-полимеразу в определенных участках генома, что может играть важную роль в изменении активности генов и «починке» ДНК, поврежденной радиацией. Похожие механизмы регуляции активности РНК-полимеразы могут действовать и у многоклеточных организмов». Работа была опубликована в журнале PNAS.
Как радиация вредит клетке
Открыты Deinococcus radiodurans были случайно: в 1956 году их нашли «в добром здравии» в банке с мясными консервами, которые пытались простерилизовать с помощью радиации.
В норме любое ионизирующее излучение — поток заряженных или нейтральных частиц или квантов, который способен превращать нейтральные атомы в заряженные ионы, возбуждая их, — разрушает гармонию слаженного механизма химических превращений, которые происходят в живой клетке.
Непреодолимые химические силы начинают тянуть ионизированные атомы к «соседям», к которым в невозбужденном состоянии они были абсолютно «равнодушны». Даже безопасные и вездесущие нейтральные молекулы воды могут превратиться в пероксид и затем в супероксид — опасные свободные радикалы, один из основных источников повреждений биологических молекул в клетке. Действие свободных радикалов называют оксидативным стрессом, так как оно связано с окислением биомолекул.
Результат — случайные химические связи, молекулярная неразбериха и «разрушение традиционных ценностей». Внутри живой клетки главным «хранителем традиций» является ДНК, в которой в закодированном виде содержится инструкция по сборке всех ее белков, важнейших участников основных клеточных процессов. Поэтому радиация (как и многие токсичные вещества), нарушающая последовательность ДНК, несет для клеток смертельную опасность: некоторые мутации могут случайно оказаться полезными, но, если не глядя переставлять детали в исправно работающем сложном механизме, вероятность сломать его несоизмеримо выше, чем вероятность изобрести что-то хорошее.
Кроме того, в ДНК могут образовываться разрывы, мешающие считыванию кода. «Ломаются» и сами белки — особенно часто повреждается SH-группы в цистеине (одной из аминокислот — «кирпичиков», из которых строится молекула белка), что нарушает их функции.
Восстать из радиоактивного пепла
Как же бактерии выживают в таких условиях? Повреждения ДНК живых организмов не всегда приводят к плачевным последствиям. В клетках есть специальные механизмы репарации — «ремонта» драгоценной молекулы, например одну из ее цепей можно достроить, «подглядывая» во вторую на том же участке и подбирая нуклеотиды («буквы» генетического кода) по принципу комплементарности, то есть подставляя на место отсутствующего фрагмента парные ему «буквы».
ДНК Deinococcus radiodurans упакована в две кольцевые хромосомы и две плазмиды — сравнительно маленькие дополнительные кольцевые молекулы ДНК. Каждая такая молекула представлена в количестве от четырех до десяти копий в любой момент жизни клетки, поэтому запасных вариантов для «сверки» у нее всегда много (а не всего две, как у нас в соматических клетках). Более того, оказалось, что основная опасность для жизни дейнококка — это не повреждение ДНК (которую можно починить, используя дополнительные копии), а как раз разрушение структуры белков, занимающихся ее ремонтом.
Для «починки» разрывов в ДНК бактерия имеет дополнительные белки: одни связываются с одиночной цепью ДНК при разрыве, чтобы защитить ее от дальнейших повреждений, другие, работая как «клеточная полиция», ловят «возмутителей спокойствия», свободные радикалы, и расщепляют их.
Кроме того, у всех бактерий есть дополнительные «хитрости», позволяющие вносить корректуры прямо в ходе транскрипции — считывания «ДНК-текстов». Однако есть ли какие-то особенности этого процесса у Deinococcus radiodurans, до последнего времени было неизвестно.
Один из механизмов, который основан на работе белков Gfh и может играть роль в процессах «ремонта» ДНК и защите клеток от радиации, и был исследован российскими учеными из ИМГ РАН. «Двое из трех соавторов, включая меня самого, работают также на кафедре молекулярной биологии Биологического факультета МГУ им. М.В. Ломоносова, — сообщает Андрей Кульбачинский. — Исследования были выполнены исключительно за счет гранта РНФ, темой которого является изучение механизмов регуляции транскрипции и их возможной роли в радиоустойчивости Deinococcus radiodurans».
Хитрости редактуры
РНК-полимераза считывает информацию с ДНК, переводя ее в РНК — более короткую молекулу, которая в зависимости от последовательности будет служить матрицей для синтеза белка или выполнять еще множество функций в клетке. РНК-полимераза является также корректором или даже «главным редактором», исправляющим ошибки этого «перевода» (транскрипции).
Ведущий автор работы рассказал, какую роль в этом процессе могут играть изученные командой российских исследователей белки Gfh-факторы. Эти белки были обнаружены только у экстремофильных (живущих в неблагоприятных, с нашей точки зрения, условиях — при высоких температурах, давлении и др.) бактерий из группы Deinococcus-Thermus, которые очень устойчивы к нагреванию и другим стрессовым воздействиям.
«РНК-полимераза — один из самых консервативных ферментов в эволюции, и структура его во многом похожа и у бактерий, и у человека. В то же время различные организмы используют самые разнообразные способы регуляции работы этого фермента.
Одной из наиболее интересных групп регуляторных факторов являются белки, которые способны напрямую воздействовать на активный центр РНК-полимеразы. Для этого они связываются в специальном канале, который соединяет поверхность РНК-полимеразы с активным центром (так называемый вторичный канал — в отличие от первичного, в котором происходит связывание ДНК и РНК)», — рассказывает Андрей Кульбачинский.
По словам ученого, у большинства бактерий встречаются Gre-белки, относящиеся к этой группе. Они могут переключать активность РНК-полимеразы, в результате чего уже «прочитанный» фрагмент (транскрипт) расщепляется. Это свойство позволяет исправлять уже сделанные в ходе транскрипции ошибки. После такой «редактуры» РНК может синтезироваться дальше. У эукариот (в том числе у человека) тоже существуют аналоги таких белков, только эволюционное происхождение они имеют иное. Это говорит об исключительной важности такого процесса.
«Исследованные нами факторы — Gfh-белки — являются родственниками (гомологами) Gre-факторов. Однако вместо того, чтобы переключать активности РНК-полимеразы, они ее ингибируют! Причем у той бактерии, которую мы исследуем (Deinococcus radiodurans), это происходит только в определенных участках генома и только в присутствии ионов марганца, которые, как уже довольно давно известно, играют роль в защите клеток дейнококка от окислительного стресса», — сообщает ученый.
Перспективы: помогут ли Gfh-факторы «бороться с бактериями их же оружием»?
Исследователи сделали предположение, что Gfh-белки могут «фиксировать» РНК-полимеразу в определенном структурном состоянии, останавливая ее ход по молекуле ДНК. Такую «замершую над ошибкой» РНК-полимеразу узнают другие белки — факторы репарации («починки») и репликации (воспроизведения) ДНК. Дальнейшей задачей ученых станет исследование роли Gfh-белков в защите дейнококков от радиации.
«Наша работа носит прежде всего фундаментальный характер: впервые обнаружено, что регуляторные факторы способны значительно усиливать паузы и терминацию транскрипции, связываясь во вторичном канале РНК-полимеразы. Так как строение РНК-полимеразы очень консервативно, весьма вероятно, что данный способ регуляции может действовать у самых разных организмов (например, и у нас с вами), только с участием других регуляторных факторов», — комментирует Андрей Кульбачинский.
Автор добавляет, что возможно и практическое применение результатов исследования. Так как Gfh-факторы фиксируют РНК-полимеразу и останавливают транскрипцию, то, изучив их, можно создать или найти другие молекулы, способные помешать бактериям переписывать информацию с ДНК на РНК и синтезировать белки. РНК-полимераза медленно изменяется с течением времени, поэтому у бактерий она очень похожа и ее удобно использовать как мишень для антибактериальных препаратов. Так, антибиотик рифампицин, используемый в борьбе с палочкой Коха, вызывающей туберкулез, подавляет именно РНК-полимеразу бактерий (правда, со временем они вырабатывают к нему устойчивость, что делает получение новых антибиотиков важнейшей проблемой ближайшего будущего).
Автор: Екатерина Мищенко