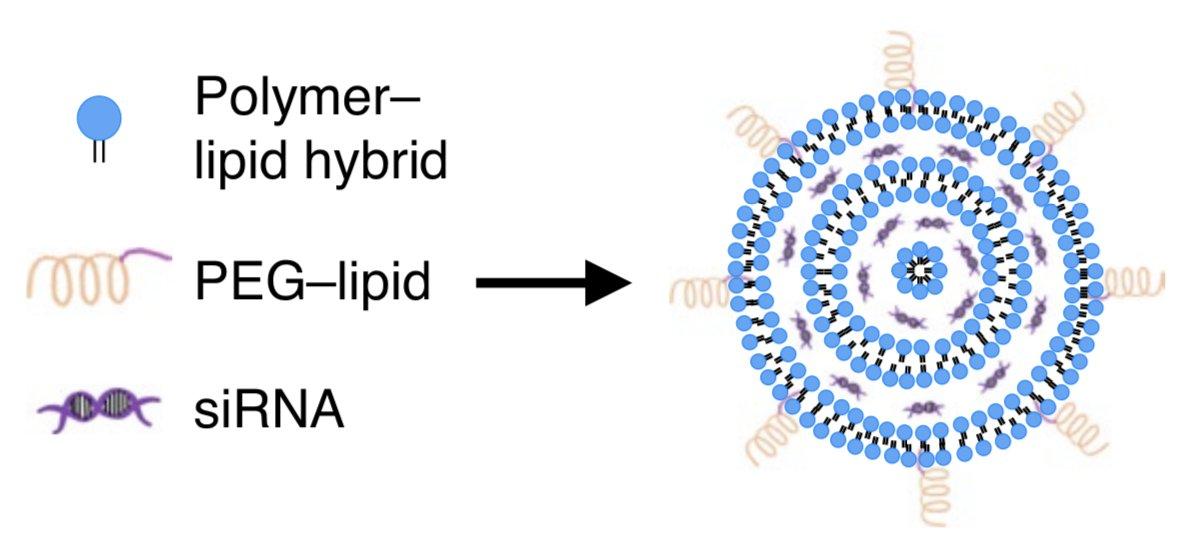
Американские ученые разработали липид-полимерные наночастицы, несущие малые интерферирующие РНК и способные проникать в клетки стромы костного мозга.
Подавляя там экспрессию различных генов, исследователи смогли управлять процессами миграции стволовых и прогениторных клеток из костного мозга в кровоток. Результаты исследования опубликованы в журнале Nature Biomedical Engineering.
В костном мозге человека находится внушительное количество прогениторных и гемопоэтических стволовых клеток, а в кровоток ежедневно высвобождается множество клеток крови. Процессы их дифференциации, пролиферации и миграции частично регулируются микроокружением стволовых клеток — стромой костного мозга, или нишевыми клетками. К ним относятся эндотелиальные клетки костного мозга, образующие тонкие однослойные кровеносные сосуды, и способные самостоятельно выделять сигнальные молекулы для кроветворных клеток.
Перспектива управления процессами миграции гемопоэтических клеток в кровоток очень привлекательна для медицины. Индукция высвобождения клеток костного мозга необходима при трансплантации стволовых клеток из периферической крови — эта процедура гораздо безопаснее и относительно безболезненная для донора, в отличие от непосредственной пересадки костного мозга. Однако не менее интересен и обратный процесс — ингибирование миграции клеток крови, так как их повышенное количество в кровотоке связывают с чересчур тяжелым течением воспалительных процессов.
Дэниел Андерсон (Daniel Anderson) и Матиас Нарендорф (Matthias Nahrendorf) из Массачусетского технологического института и Массачусетской больницы общего профиля вместе с коллегами в поисках решения этих вопросов решили подавить экспрессию некоторых генов в эндотелиальных клетках стромы костного мозга мышей с помощью малых интерферирующих РНК (siRNA), доставляемых в составе наночастиц.
Для создания наночастиц ученые использовали С15-липиды с эпоксидной группой на одном конце и низкомолекулярные полиамины в молярном соотношении 14:1. Получившийся материал смешали с siRNA и полиэтиленгликолем, после чего частицы образовались за счет электростатических взаимодействий между положительно заряженным полимером и отрицательно заряженными нуклеиновыми кислотами.
В качестве рычагов управления процессами миграции клеток авторы решили воспользоваться белками-хемокинами SDF-1 (stromal cell-derived factor-1) и MCP-1 (monocyte chemoattractant protein-1). Первый из них обеспечивает локализацию гемопоэтических стволовых клеток в строме костного мозга, не допуская ранней миграции из нее, второй — наоборот, отвечает за выход клеток и их транспорт в очаги воспаления. Цель заключалась в том, чтобы, подавляя экспрессию этих генов с помощью соответствующих малых интерферирующих РНК, искусственно вызвать выход гемопоэтических клеток из костного мозга, либо заставить их там оставаться.
В экспериментах in vivo мышам внутривенно вводили липид-полимерные наночастицы с siSdf1 (siRNA, направленная на подавление экспрессии гена Sdf1) и наблюдали за последствиями. Оказалось, что в крови повысилось количество LSK клеток (lineage− sca1+ c-kit+) — ранней формы гемопоэтических клеток у мышей. Также ученые обратили внимание на выход из костного мозга, помимо стволовых клеток, моноцитов и нейтрофилов — их количество в крови мышей также было повышено.
То же проделали с наночастицами, содержащими уже siMcp1. Высокая экспрессия Mcp1, как правило, связана с инфекциями — MCP-1 секретируется в нишу стволовых клеток и обеспечивает выход моноцитов в кровоток для борьбы с патогеном. По этой причине авторы, после введения липид-полимерных наночастиц с siMcp1 в кровь мышам, ввели им также липополисахариды (характерный бактериальный антиген). В результате экспрессия Mcp1 в контроле была действительно высокой, в отличие от группы, которой ввели наночастицы с siMcp1. При этом ожидаемо возросло количество моноцитов в строме костного мозга, а в кровотоке — напротив, уменьшилось.
За результатами этой работы авторы видят большой потенциал в лечении онкологических заболеваний, а также воспалительных процессов. В частности, при инфаркте миокарда последующее за этим повышение количества моноцитов, концентрирующих на пораженных тканях сердца, может вызывать осложнения. Предложенный метод подавления экспрессии хемокинов нишевых клеток костного мозга подходит для их предотвращения.
РНК-интерференция — сравнительно простой метод подавления экспрессии определенного гена в клетках практически любой ткани. Вопрос обычно заключается в доставке интерферирующей РНК, минуя многочисленные эндонуклеазы крови. Не так давно FDA одобрило второе в мире лекарство на основе РНК-интерференции и оно, вероятно, не будет последним.
Автор: Наталия Миранда