Французские и американские ученые сообщили о первом случае излечения человека от серповидноклеточной анемии с помощью генной терапии. Пациентом стал подросток из Франции. Описание случая приводится в New England Journal of Medicine.
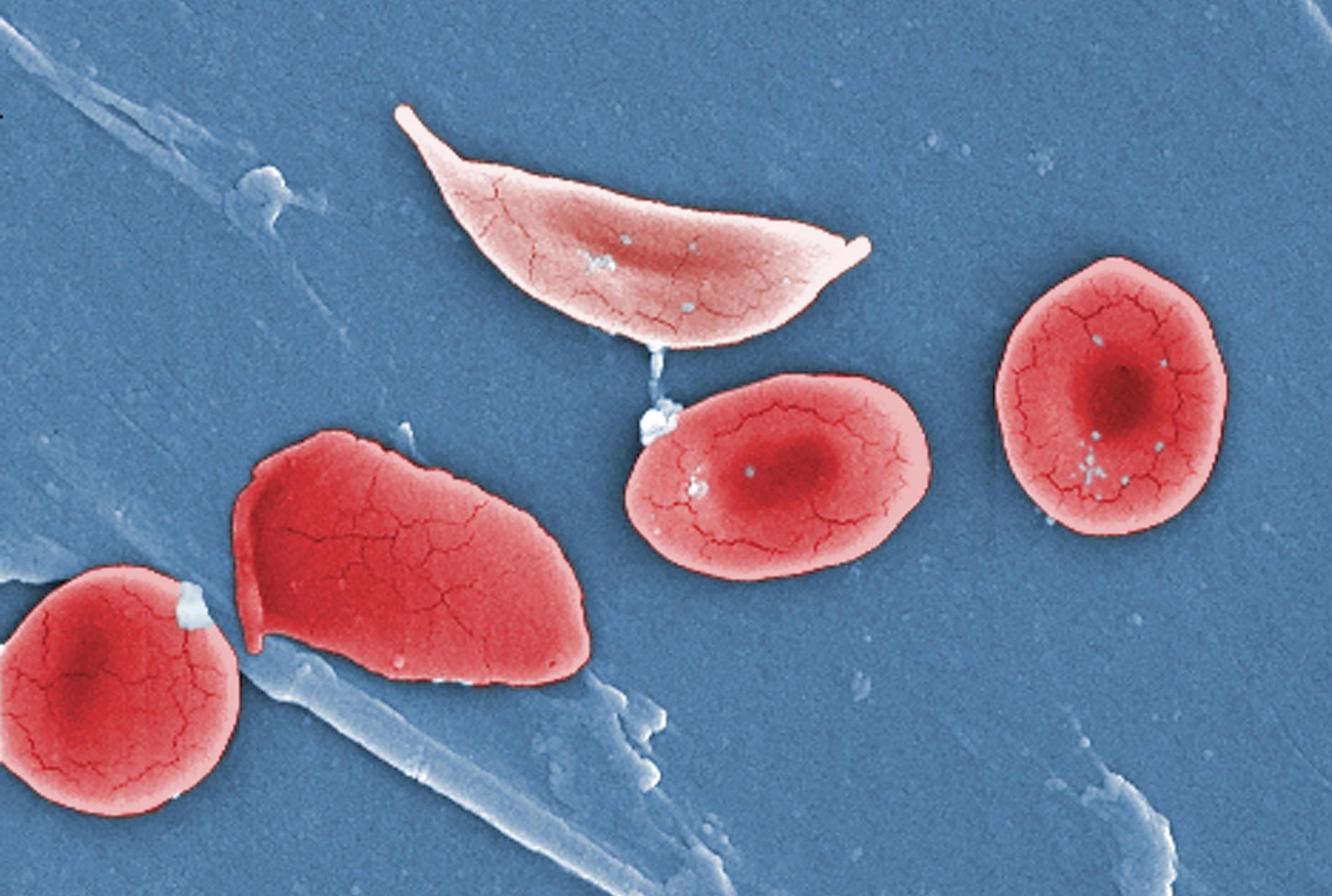
Серповидноклеточная анемия — это наследственное заболевание, обусловленное одиночной мутацией в гене бета-субъединицы гемоглобина (белковая часть гемоглобина состоит из двух альфа- и двух бета-субъединиц). Дефектный гемоглобин (HbS), отдавая тканям кислород, полимеризуется с образованием волокон, которые деформируют эритроциты, придавая им серповидную форму. Такие эритроциты хуже проходят через мелкие сосуды, что приводит к образованию тромбов, а также быстрее разрушаются, из-за чего возникает анемия.
Для лечения серповидноклеточной анемии в настоящее время одобрено только одно лекарство — гидроксимочевина. Она способствует синтезу младенческой (фетальной) формы гемоглобина, которая снижает концентрацию HbS и замедляет его полимеризацию. Однако препарат действует не на все клетки и обладает множеством побочных эффектов. Небольшому числу пациентов (примерно 18 процентам) можно помочь пересадкой донорского костного мозга. Подобные виды лечения не могут покрыть потребности всех больных, и ученые на протяжении десятков лет занимались разработкой генной терапии заболевания. После успешных ее испытаний на животных в 2014 году начались клинические испытания этого метода лечения.
Одним из участников испытаний, которые продолжаются до сих пор на базе Детской больнице Неккер в Париже, стал мальчик, болевший серповидноклеточной анемией с рождения и наблюдавшийся в этом медучреждении. В возрасте от двух до девяти лет пациент получал гидроксимочевину без выраженного эффекта: у него наблюдались повторные тромбозы мелких сосудов (в том числе дважды — легочных) и двусторонний очаговый некроз бедренных костей. С 2010 года ему проводили профилактические переливания эритроцитарной массы.
В октябре 2014 года, когда мальчику было 13 лет, ему провели генную терапию в соответствии с протоколом, разработанным французскими учеными и американской компанией Bluebird Bio. На первом этапе лечения у пациента дважды забрали ткань костного мозга (для проведения терапии и создания резервного запаса) и выделили из нее мультипотентные кроветворные клетки (CD34+). В эти клетки с помощью обезвреженного лентивируса ввели ген здорового варианта бета-глобина βA-T87Q. Средняя доза геннотерапевтического препарата LentiGlobin BB305 составила 1,0 и 1,2 копии вирусного вектора на клетку.
После этого мальчику провели миелоабляцию (уничтожение кроветворных клеток) бусульфаном. Через два дня ему ввели модифицированные клетки. На всем протяжении лечения пациенту переливали кровь, пока уровень βA-T87Q не достиг от 25 до 30 процентов от всего гемоглобина на 88 день терапии.
На шестой месяц уровень общего гемоглобина в крови мальчика стабилизировался на показателях от 106 до 120 граммов на литр (около нижней границы нормы). К девятому месяцу после введения модифицированных клеток βA-T87Q составлял 46 процентов, а к 15 месяцу — 48 процентов от всего гемоглобина.
В течении более чем 15 месяцев наблюдения у пациента не наблюдалось никаких клинических событий, связанных с серповидноклеточной анемией, показатели анализа крови нормализовались. По итогам наблюдения всю медикаментозную терапию отменили за ненадобностью. Основные побочные эффекты были связаны с миелоабляцией и устранены в процессе лечения.
Помимо описываемого пациента к настоящему времени терапию препаратом LentiGlobin BB305 получили еще несколько десятков французских и американских участников испытаний с серповидноклеточной анемией и другим наследственным дефектом бета-глобина — бета-талассемией. Предварительные результаты лечения признаны обнадеживающими, однако окончательные выводы делать пока рано, пишут авторы работы.
Недавно были разработаны несколько других экспериментальных подходов к терапии серповидноклеточной анемии и других гемоглобинопатий. В частности, ученые успешно испытали на мышах и клетках человека редактирование дефектного гена с помощью системы CRISPR/Cas9, убедились, что вещества, увеличивающие объем эритроцитов, препятствуют их деформации, и разработали метод генетической коррекции мутаций гемоглобина, основанный на пептидонуклеиновых кислотах.
Автор: Олег Лищук