Биологи из США обнаружили, что ингибирование фермента фосфоинозитол-3-киназы, участвующего в передаче внутриклеточных сигналов, снижает уровень клеточной гибели и предотвращает выброс клеткой медиаторов воспаления. Статья опубликована в Nature Communications.
Число клеток в организме регулируется балансом между клеточным делением и клеточной гибелью. Поддержание постоянства числа клеток очень важно для нормального функционирования тканей и предотвращения развития опухолей. Гибель клеток также возникает при патологических состояниях: например, при проникновении в организм патогенов. Обычно патогены в первую очередь поражают внутреннюю выстилку сосудов — эндотелий. Содержимое поврежденных клеток выбрасывается в кровь, что может приводить к осложнению инфекции неконтролируемым воспалительным ответом. Подобное состояние возникает при остром респираторном дистресс-синдроме.
Существует множество видов клеточной гибели. Один из них — пироптоз — не всегда приводит к гибели клетки. В запуске пироптоза участвует белок газдермин D. В активированном состоянии он формирует поры в цитоплазматической мембране, что приводит к проникновению кальция внутрь клетки, активации ключевых ферментов клеточной гибели — каспаз, а также к высвобождению провоспалительных цитокинов. Причина обратимости пироптоза неизвестна, но может скрываться в динамике открытия и закрытия пор из газдермина D.
Чтобы изучить динамику пор из газдермина D биологи из Иллинойсского Университета в Чикаго во главе с Аной Беатрис Санта Крус Гарсиа (Ana Beatriz Santa Cruz Garcia) создали трансгенный белок, активирующийся под действием света. Активированный газдермин D формировал поры, что приводило к поступлению внутрь клетки ионов кальция и запуску пироптоза. Изучение динамики пор на искусственной мембране показало, что поры способны спонтанно открываться и закрываться.
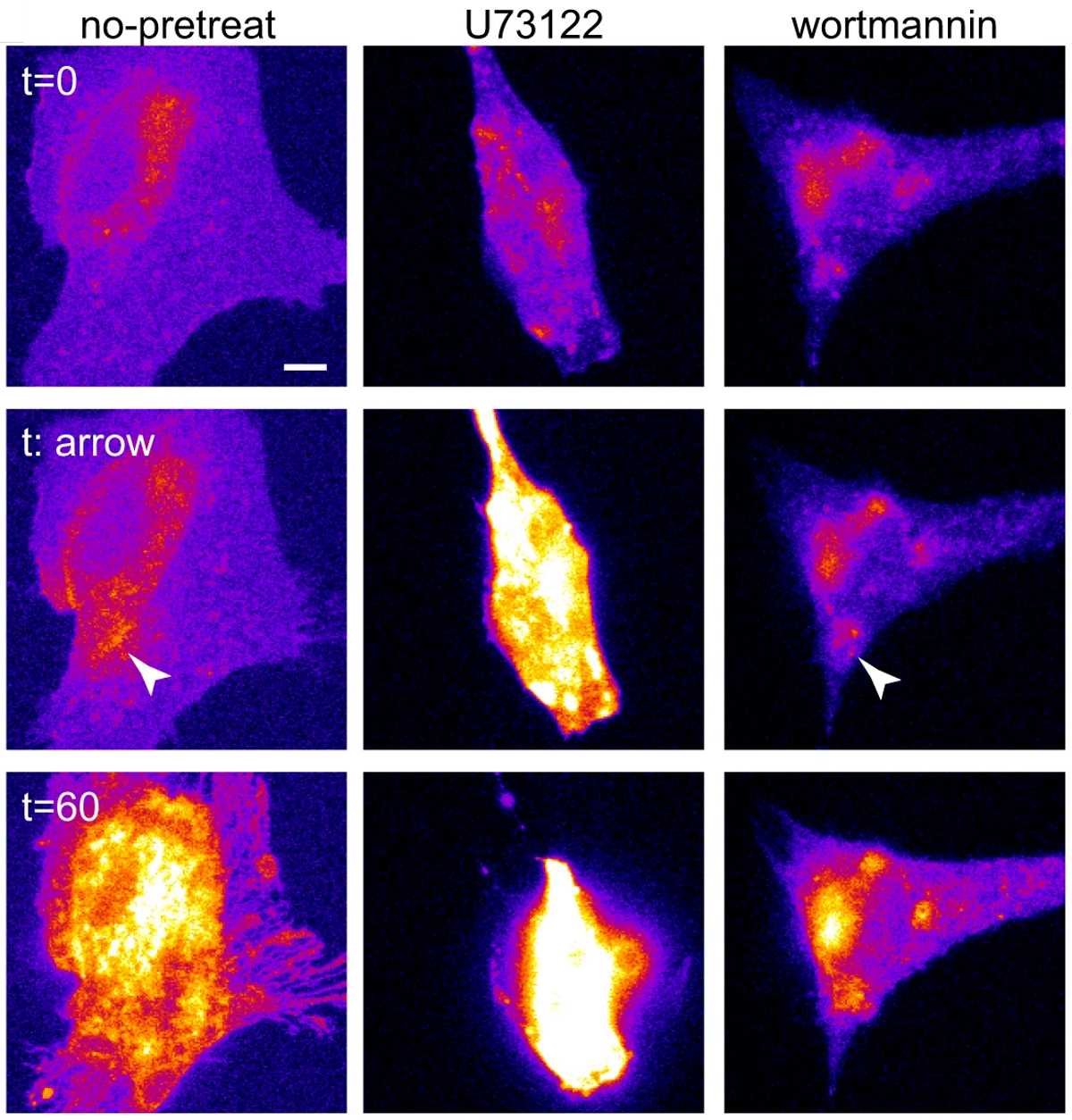
Ранее предполагали, что для функционирования пор из газдермина D цитоплазматическая мембрана клетки должна содержать в своем составе фосфатидилинозитол — липид, участвующий в передаче внутриклеточных сигналов. В передаче сигнала также участвуют два фермента: фосфолипаза C и фосфатидилинозитол-3-киназа. Чтобы изучить роль PLC и PI3K в пироптозе, ученые использовали химические ингибиторы этих киназ — U73122 и вортманнин, соответственно. Эксперимент проводили на клетках линии HeLa. Маркером запуска пироптоза служил приток ионов кальция в клетку. Добавление ингибитора PLC U73122 вызывало усиленный по сравнению с контролем приток кальция в клетку. Ингибирование PI3K с помощью ворманнина, напротив, приводило к снижению уровня кальция по сравнению с контролем, стимулируя закрытие пор.
Помимо притока ионов кальция, ингибиторы PLC и PI3K влияли на выработку провоспалительного цитокина интерлейкина-1β мышиными макрофагами. Продукцию цитокина стимулировали добавлением в среду липополисахаридов (компонентов мембран грамотрицательных бактерий). Добавление U73122 на фоне ЛПС повышало уровень интерлейкина-1β, а добавление вортманнина — снижало.
Мы уже рассказывали, что другой вид клеточной смерти — апоптоз — связан с пониженной частотой возникновения опухолей у галапагосских черепах.
Автор: Наталья Кондратенко