Американские ученые успешно проверили в экспериментах на мышах метод «точечной» блокировки иммунной реакции в области мозга, пораженной ишемическим инсультом.
Такая блокировка предотвращает посттравматическую воспалительную реакцию и снижает риск тяжелых поражений и инвалидности, говорится в статье, опубликованной в Science Translational Medicine.
В России в год диагноз «ишемический инсульт» ставят 550 тысячам людей, умирают от него ежегодно около 200 тысяч человек и еще около 47 тысяч становятся инвалидами. Постинсультная реабилитация занимает многие месяцы, и не всегда человек может полностью восстановиться. Причиной этого становится в том числе воспаление нервных тканей мозга после инсульта, во время которого гибель клеток продолжается как минимум в течение месяца после устранения ишемии.
Исследователи под руководством Стивена Томлинсона (Stephen Tomlinson) из Медицинского университета Южной Калифорнии выяснили, что появляющиеся в поврежденных тканях неоэпитопы (индуцированные ишемией и связанные с повреждением молекулярные агенты, DAMPs) через связь с IgM (иммуноглобулин М) активируют систему комплемента — комплекс сигнальных элементов иммунной системы, содержащихся в крови. Одни из частей комплемента — опсонины — «метят» части погибших нейронов, а также нейроны так называемой пенумбры или зоны «оглушения», которые еще пока живы и могут восстановить свою функцию с появлением нормального кровоснабжения. «Помеченные» клетки и их части привлекают на себя микроглию, которая обладает фагоцитарной активностью и их утилизирует. Однако, если локально подавить работу комплемента, то микроглия не активируется и фагоцитоза не происходит, из-за чего оглушенные клетки остаются сохранными.
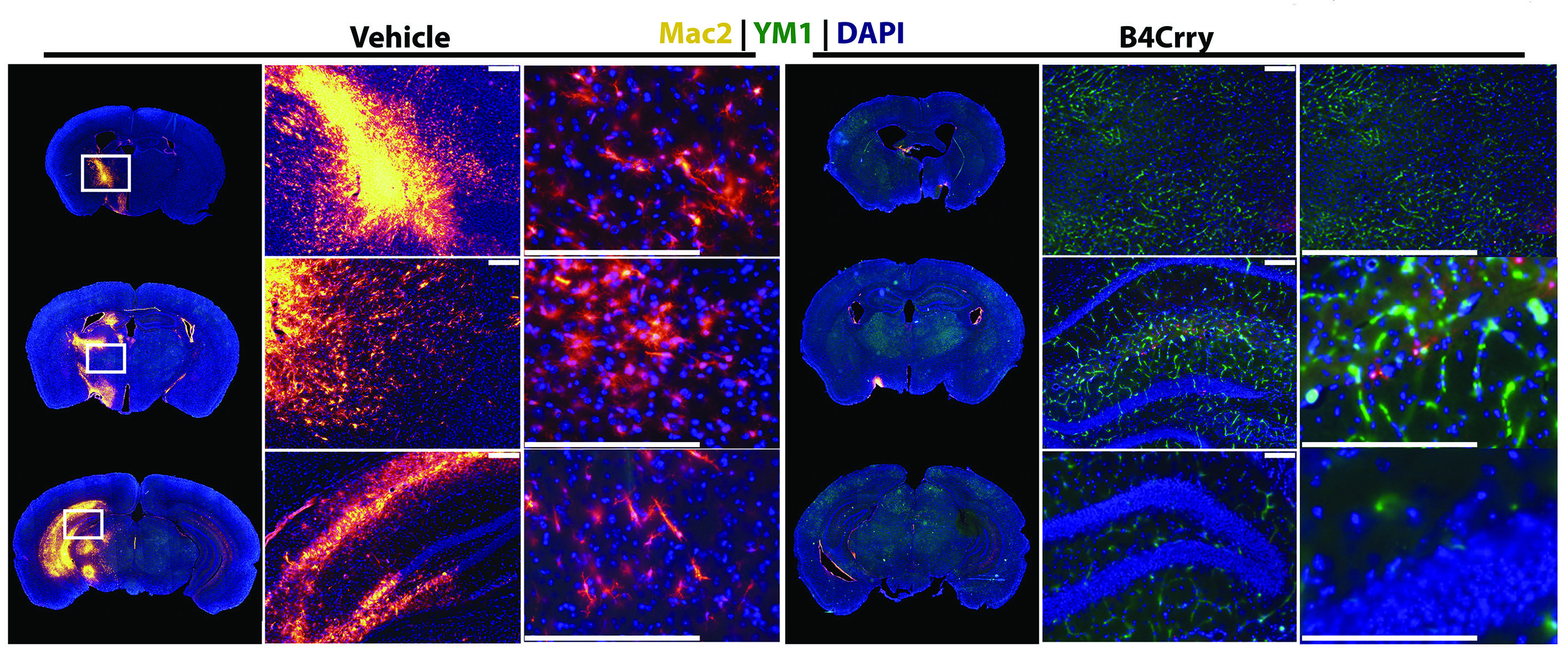
Команда ученых основывалась на своей прошлой работе, где уже выявили связь запуска системы комплемента с объемом постишемического повреждения. Она создала молекулярный комплекс, где совместила ингибитор комплемента — мышиный аналог человеческого рецептора комплемента 1 (CR1), который подавляет весь каскад активации системы — и одноцепочечное моноклональное антитело, связывающееся с неоэпитопом в эпицентре поражения. Комплекс назвали B4Crry.
Сначала действие терапевтического комплекса проверили на культуре мышиных эндотелиальных клеток мозга в модели кислородно-глюкозной депривации. Выяснилось, что после реоксигенации он хорошо блокирует нежелательную активацию комплемента.
Затем перешли к экспериментам на животных. У лабораторных мышей с помощью операции моделировали окклюзию средней мозговой артерии, а затем через 2 или 6 часов однократно вводили лечебный комплекс и наблюдали за эффектом.
С помощью радиометки ученые показали, что после введения B4Crry специфически связывался с поврежденными тканями ипсилатерального полушария (там, где было нарушение) даже в том случае, если окклюзию средней мозговой артерии произвели 2 часа назад. При этом локализация препарата в других органах и в контралатеральном полушарии оставалась минимальной, а у контрольных животных с фиктивной травмой препарат и вовсе не накапливался. Также авторы доказали, что блокировались только те компоненты комплемента, которые провоцируют воспаление.
Активность вещества оказалась максимальной через 24 часа после окклюзии. Это явление они связали с увеличением проницаемости гематоэнцефалического барьера (ГЭБ), учитывая, что обнаружили также и положительную корреляцию между специфической активностью B4Crry и степенью проницаемости ГЭБ. Период полураспада препарата составил около 35 часов.
За восстановлением животных наблюдали в течение 15 дней. Мыши, подвергшиеся лечению B4Crry, страдали менее выраженными неврологическими проявлениями, а размер поражения их мозга, по сравнению с группой контроля, которой вводили растворитель (vehicle), оказался гораздо меньше: вовлечение коры и гиппокампа было минимальным, а зона инфаркта за 15 дней существенно регрессировала. За этот же период времени их когнитивные (в том числе память, обучаемость) и двигательные функции восстановились в большем объеме, нежели в контрольной группе.
Но главное — то, что вещество, если его вводили даже через 24 часа после окклюзии, показывало эффект, сопоставимый с терапией активаторами тканевого плазминогена, которые вводили в диапазоне от 3 до 4,5 часов от начала острой ишемии. А эти препараты на сегодняшний день — единственный одобренный и эффективный фармакологический агент для терапии инсульта (правда, с очень узким терапевтическим окном).
Таким образом, исследователи показали, что за локальным ингибированием системы комплемента, запускающей нейровоспаление, стоит будущее лечения ишемического инсульта и постинсультной реабилитации.
Тем временем, другие ученые уже выяснили, что уменьшение воспалительной реакции с помощью блокировки цитокина интерлейкина-1 помогает тканям мозга частично восстанавливаться. Ну а регулярное посещение сауны может снизить риск возникновения инсульта среди пожилых людей на 61 процент.
Автор: Анна Хоружая