Американские нейробиологи из Пенсильванского университета, Юго-западного медицинского центра UT и Лаборатории Джексона выяснили, что физические упражнения улучшают выносливость не только через перестройку мышц, сердечно-сосудистой и метаболической систем, но и через обязательное участие определенной группы нейронов головного мозга.
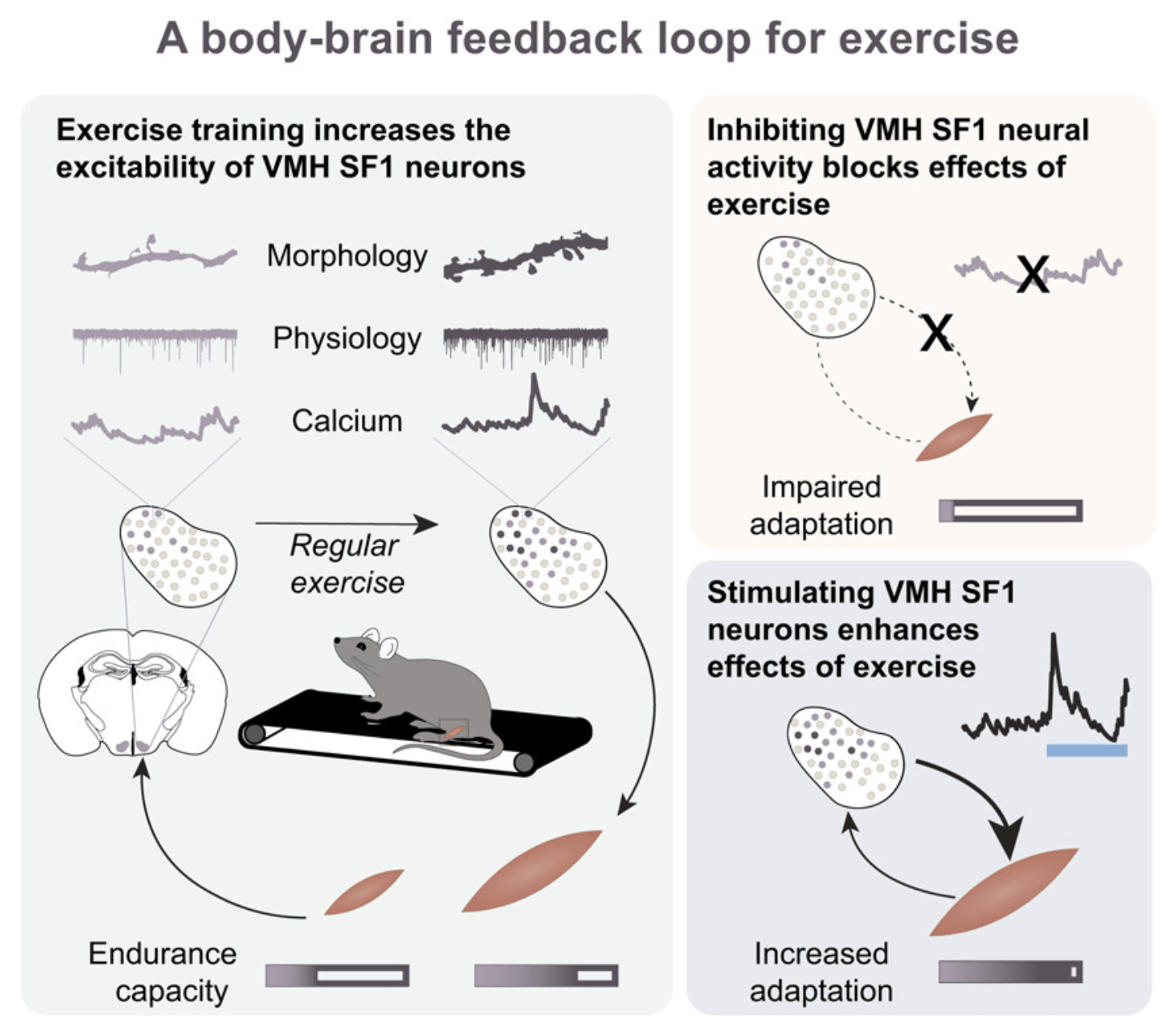
Оказалось, что нейроны вентромедиального гипоталамуса (ВМГ), производящие стероидогенный фактор-1 (SF1), активируются после каждой тренировки, и именно эта активация запускает каскад периферических адаптаций, делающих нас сильнее и выносливее. Без работы этих клеток физические упражнения не дают никакого тренировочного эффекта – мышцы не перестраиваются, выносливость не растет. Более того, искусственная стимуляция SF1-нейронов после занятий способна усилить тренировочный эффект сверх обычного. Исследование опубликовано в журнале Neuron.
До сих пор периферическое звено в адаптации к нагрузкам считалось ключевым: регулярные тренировки улучшают выносливость за счет перестройки скелетной мускулатуры, сердечно-сосудистой, эндокринной и иммунной систем. Нейронные изменения в мозге – нейрогенез, усиление синаптической связности, снижение нейровоспаления – рассматривались как следствие, а не причина роста выносливости. Вентромедиальный гипоталамус давно известен как структура, регулирующая энергетический гомеостаз: SF1-нейроны объединяют периферические метаболические сигналы (лептин, инсулин, глюкозу) и управляют расходом энергии. Генетические эксперименты указывали, что снижение экспрессии SF1 нарушает прирост выносливости, но механизм оставался неизвестным.
В новом исследовании применялся широкий арсенал современных нейробиологических методов на мышах. Активность SF1-нейронов блокировали с помощью тетанотоксина. Для мониторинга нейронной активности в реальном времени применяли генетически кодируемый кальциевый индикатор в сочетании с кальциевой визуализацией – метод, позволяющий следить за активностью одних и тех же отдельных нейронов в разные дни тренировок. Электрофизиологические свойства SF1-нейронов исследовали как у тренированных, так и у малоподвижных мышей. Для причинно-следственного анализа использовали двунаправленную оптогенетику: по окончании каждой тренировочной сессии SF1-нейроны либо подавляли, либо активировали световыми импульсами. Тренировочный протокол включал беговые дорожки и добровольный бег в колесе, выносливость оценивалась в тестах «до истощения» и стресс-тестах с нарастающей скоростью.
Уже после одной тренировки в ВМГ повышалась экспрессия мозгового нейротрофического фактора, причем как доля SF1-нейронов, его производящих, так и количество транскриптов (на основе которых «строился» белок) на клетку возрастали. Ученые выявили два функционально различных подтипа SF1-нейронов: «подавляемые после бега» и «активируемые после бега». Именно вторая группа оказалась ключевой: после недели тренировок число включающихся после нагрузки нейронов значимо возросло, а амплитуда их ответов увеличилась. Отслеживание одних и тех же клеток в динамике подтвердило, что это не набор новых нейронов, а усиление активности уже существующих.
Функциональные эксперименты окончательно укрепили причинно-следственные связи. Мыши, у которых SF1-нейроны «заглушались» тетанотоксином, имели сопоставимое с контролем максимальное потребление кислорода (VO₂max), однако обладали сниженной выносливостью и скоростью в стресс-тестах. После нескольких недель тренировок транскрипционные изменения в скелетных мышцах, характерные для нормальной адаптации, у таких мышей остались практически полностью подавленными, и роста выносливости не наблюдалось.
Оптогенетическое затормаживание SF1-нейронов именно в период после тренировки (но не во время нее) воспроизводило такой же эффект: прирост выносливости блокировался, а нормальное посттренировочное повышение глюкозы крови не происходило. Напротив, оптогенетическая активация SF1-нейронов сразу после тренировки, когда животные уже достигли плато производительности, давала дополнительный прирост выносливости сверх того, что обеспечивали сами тренировки. Стимуляция SF1-нейронов также увеличивала общий расход энергии, потребление кислорода и долю углеводов в субстрате окисления.
Авторы в качестве объяснения предлагают модель «прямой связи» (feed-forward): активированные тренировкой SF1-нейроны подвергаются пластическим изменениям, которые, в свою очередь, запускают их ответ на следующую нагрузку. Мозг «запоминает» историю физической активности через структурную и функциональную перестройку синаптических входов. Вероятно, активированные SF1-нейроны повышают глюкозу в крови, запуская восполнение гликогена и транскрипционную программу в мышцах через те молекулярные события, которые традиционно приписывались исключительно периферическим сигналам.
Конечно, исследование проведено только на мышах, и перенос результатов на человека требует отдельной проверки. Остается также неизвестным, какие именно периферические сигналы из мышц, печени или других органов активируют SF1-нейроны после нагрузки. Требует дальнейшего изучения и функциональная специфичность подтипов SF1-нейронов (реагируют на нагрузку или на социальные взаимодействия тоже).
Тем не менее авторы прямо указывают, что понимание роли SF1-нейронов открывает принципиально новый путь к созданию «имитаторов упражнений» – фармакологических или технологических инструментов, активирующих эту нейронную цепь у людей, которые не могут заниматься физической активностью из-за болезни, травмы или инвалидности. Если нейронная активация после нагрузки – действительно необходимое и достаточное условие для получения тренировочного эффекта, то воздействие непосредственно на эту мозговую цепь может стать альтернативой самим упражнениям – по крайней мере, в части метаболических и мышечных адаптаций.
Текст: Анна Хоружая