Хроническая мигрень является тяжелым видом головной боли, зачастую сложно поддающимся лечению. В новом исследовании ученные из Пекина смогли в очередной раз «приоткрыть завесу» патофизиологии этого заболевания, смоделировав симптомы мигрени и связанной с ней тревоги у крыс.
Главным фокусом наблюдений была выбрана кора островковой доли, в которой обнаружены повышенная экспрессия белков c-Fos и CGRP и рецепторов NMDA, содержащих GluN2B субъединицу. Оказалось, что введение напрямую в островковую кору блокатора аденилатциклазы 1 hNB001 снижало экспрессию этих белков и симптомы мигрени у крыс. Подобный эффект наблюдался также при внутрибрюшинном введении, что обусловлено прохождением hNB001 через гематоэнцефалический барьер. Статья опубликована в журнале The Journal of Headache and Pain.
Мигрень считается хронической при возникновении приступов головной боли 15 дней в месяц и чаще. От хронической мигрени (ХМ) страдает около 2% населения. Это заболевание занимает второе место в мире среди причин утраты работоспособности.
Несмотря на большое количество исследований в сфере хронических болей и мигрени, многие звенья патогенеза этих состояний до сих пор остаются загадкой. С каждым годом происходят все новые открытия в этой области, а бурное развитие фармакологии позволяет разрабатывать лекарственные средства, направленные на различные элементы, участвующие в развитии боли. Так, например, для лечения хронической мигрени используются моноклональные антитела к кальцитонин-ген-связанному пептиду (CGRP), антагонисты рецепторов CGRP (гепанты), антагонисты серотониновых рецепторов (дитаны), а также препараты из других групп (антидепрессанты, противоэпилептические, антигипертензивные и прочие). Для купирования приступов мигрени используются как противовоспалительные средства, так и препараты, воздействующие на серотониновые рецепторы (триптаны). Однако, даже при таком разнообразии, у большого количества людей не удается достичь избавления от боли.
Инсулярная кора (ИК) или кора островковой доли наряду с передней поясной корой участвует в восприятии боли. Во многом ИК несет ответственность за негативные эмоции, связанные с болью. Аффективные проявления, такие как тревожное расстройство и депрессия, являются постоянным спутников ХМ и других болевых синдромов, что усиливает болевые ощущения и способствует сенситизации к боли. В предыдущих исследованиях отмечалось изменение функциональных связей между ИК и дорсальным медиальным таламусом, а также ИК с околоводопроводным серым веществом у людей с ХМ.
В новом исследовании авторы из Китая изучали особенности ИК у животных с симптомами мигрени. Для моделирования симптомов ученые проводили хирургическую операцию и устанавливали крысам канюлю, подведенную к твердой мозговой оболочке. В канюлю вводились вещества, провоцирующие боль – брадикинин, серотонин, гистамин, простагландин Е2. Кроме того, с двух сторон устанавливались канюли, подведенные к ИК.
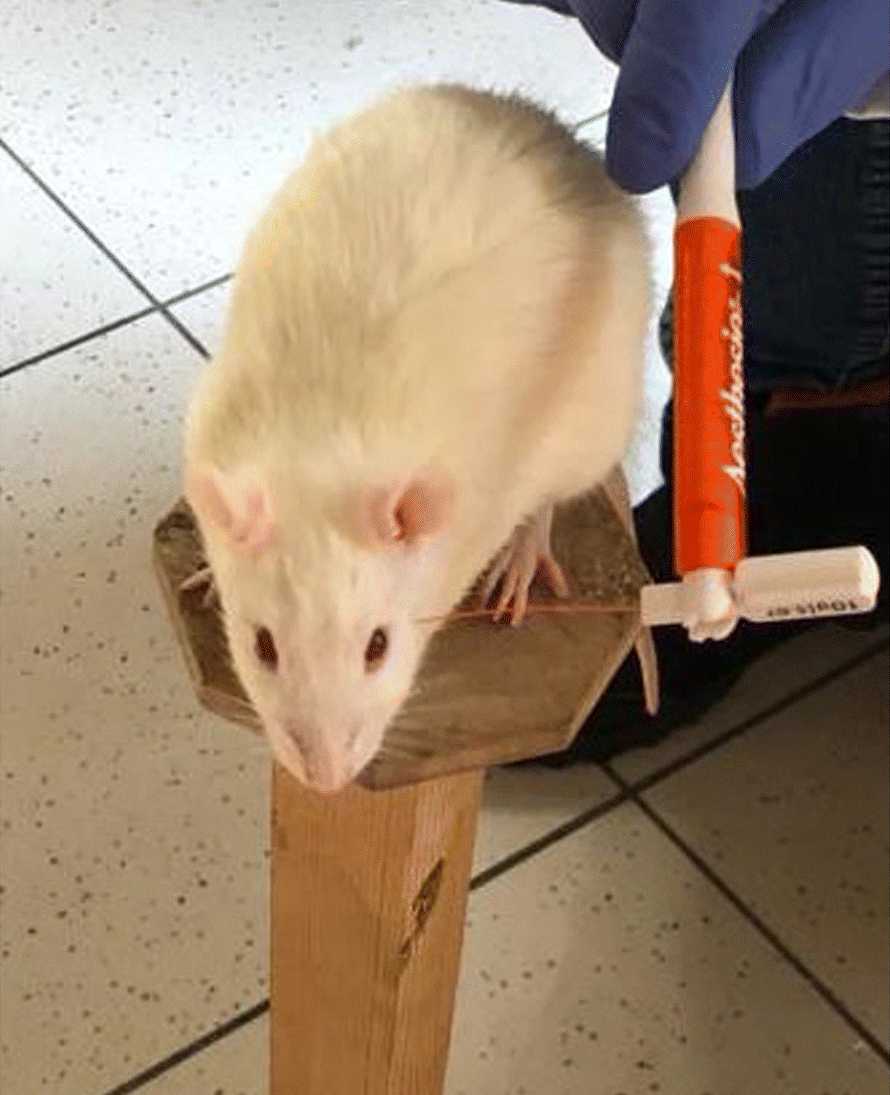
Тестирование боли происходило с использованием специального устройства: нити фон-Фрея. Нити с разной толщиной и весом прикладывали к периорбитальной области. У животных с мигренью даже слабое прикосновение способно вызвать боль. Состояние, при котором раздражители, неспособные вызвать боль в нормальных условиях, оказываются болезненными, называется аллодиния. Этот симптом встречается более чем у половины пациентов с мигренью в момент приступа.
Тест «открытое поле» использовался для оценки тревоги. Крыс помещали в центр небольшого закрытого пространства и наблюдали за их перемещениями. Животные с симптомами мигрени проводили меньше времени в центре, больше жались к стенкам и проходили меньшую дистанцию, что было интерпретировано как знаки тревоги и стресса.
Методом иммунофлюоресценции удалось выявить повышенную экспрессию белков c-Fos и CGRP в ИК у животных с симптомами мигрени. Отмечено было и повышение экспрессии рецепторов NMDA, содержащих GluN2B субъединицу у крыс с головной болью, что обусловило более частое возникновение спонтанных возбуждающих постсинаптических потенциалов в сравнении со здоровыми животными.
Аденилатциклаза 1 (Ац1) – специфичный для нервной ткани фермент внутриклеточной передачи сигнала. Предыдущие исследования показали, что Ац1 является важным «игроком» в патогенезе хронической боли, а локальное введение hNB001, ингибитора этого фермента, в переднюю поясную кору, может нивелировать симптомы мигрени.
Авторы выяснили, что локальное введение hNB001 в ИК через канюлю также значительно снижает у крыс болевые ощущения, вызванные нитью фон-Фрея, и тревогу в тесте «открытое поле». Эффекты hNB001 были опосредованы снижением экспрессии белка CGRP в ИК. Важным открытием явилось и то, что подобные результаты были достигнуты при интраперитонеальном (внутрибрюшинном) введении hNB001. Это согласуется с ранее полученными данными о прохождении hNB001 через гематоэнцефалический барьер.
Результаты, полученные группой ученых из Пекина невероятно важны для постепенного открытия все новых звеньев патогенеза хронической мигрени и других хронических болей. Ац1 может стать следующей мишенью для разработки препаратов, направленных на лечение хронических болевых синдромов. Все новые данные об эффективности hNB001 и, что немаловажно, о возможности его прохождения через гематоэнцефалический, дают надежду на скорое создание и применение лекарств на его основе.
Текст: Вадим Русскин