Ученые из Института биологических исследований Солка применили новый метод изучения процессов восстановления ДНК в нейронах и выяснили, как именно нервные клетки поддерживают целостность своей «главной информационной молекулы».
Оказалось, что существуют горячие точки, где процесс «починки» ДНК идет наиболее активно, причем они связаны с нейродегенеративными заболеваниями и «созреванием» молекул РНК, на основе которых затем строятся белки. Больше молекулярных подробностей – в журнале Science.
Дезоксирибонуклеиновая кислота или, по-простому, ДНК – основа сохранения постоянства всего живого. Она несет в себе информацию обо всех белках нашего организма и не только. Также на нас постоянно и изнутри, и извне воздействуют различные неблагоприятные условия (например, свободные радикалы, так и норовящие выбить из молекул «плохо лежащие» электроны, или же радиация), и части ДНК могут повреждаться, причем, десятки тысяч раз в день. Чтобы эти повреждения критически не сказались на жизнедеятельности клеток, в них существует противоположно направленный процесс, называемый репарацией. Ее осуществляют «специально подготовленные» ферменты, которые меняют «ошибочную» версию фрагмента ДНК на правильную.
Как правило, наиболее активно репарация происходит в делящихся клетках, например, эпителиальных или клетках соединительной ткани. Тем не менее поддержание этого процесса на должном уровне крайне необходимо и «долгожителям» нашего организма – нейронам. Но то, как в них происходит репарация, пока изучено недостаточно.
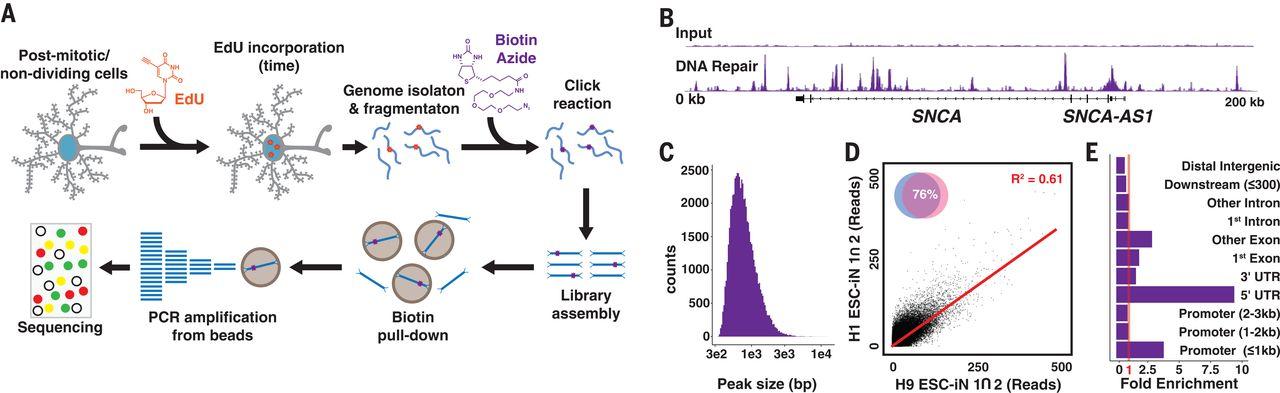
Коллектив авторов из США воспользовался методом изучения репарации ДНК, названным Repair-seq, суть которого состоит в том, чтобы в места повреждений внедрить меченый нуклеотид, а затем по нему оценить активность «работы» по восстановлению молекулы. Авторы пишут, что создали этот метод сами, но интересно, что незадолго до этого в журнале Nature вышла статья, в которой очень похожим методом также оценивалась репарация ДНК в нейронах, только немного в других ее местах. Вот она, настоящая научная гонка.
Исследователи работали с культурами нейронов, полученными из стволовых клеток человека. Результаты экспериментов оказались ожидаемыми – в нейронах действительно обнаружилось очень много мест с репарацией. Но любопытным стал факт, что они были разбросаны не случайно и сильно повторялись от клетки к клетке. Ученые назвали эти места горячими точками.
Присмотревшись к ним пристальнее, авторы выявили, что 23,5 процента горячих точек приходились на те места ДНК, на которых активно происходила транскрипция – процесс считывания информации и перевод ее в последовательность РНК. Причем, большинство их этих точек располагались в местах «запуска» транскрипции генов – промоторах. А вообще более 67 процентов мест репарации приходились именно на гены, причем, наиболее активные в нейронах.
Еще один любопытный факт, который удалось установить – то, что большинство этих генов оказались связаны с нейродегенеративными заболеваниями (в том числе болезнью Альцгеймера) и с «созреванием» молекул РНК до готовности стать основой белка – сплайсингом. Причем, многие участки репарации располагались рядом с «биологическими часами» клетки – местами метилирования ДНК. Авторы предполагают, что такое соседство со временем может привести к смещению горячих точек, а это, в свою очередь, приведет к большему накоплению ошибок в ключевых генах, поломки в которых инициируют процессы нейродегенерации.
В целом, метод Repair-seq может оказаться полезным для выявления и других закономерностей восстановления ДНК не только в нейронах, но и, например, в кардиомиоцитах, которые тоже считаются клетками-долгожителями.
Текст: Анна Хоружая