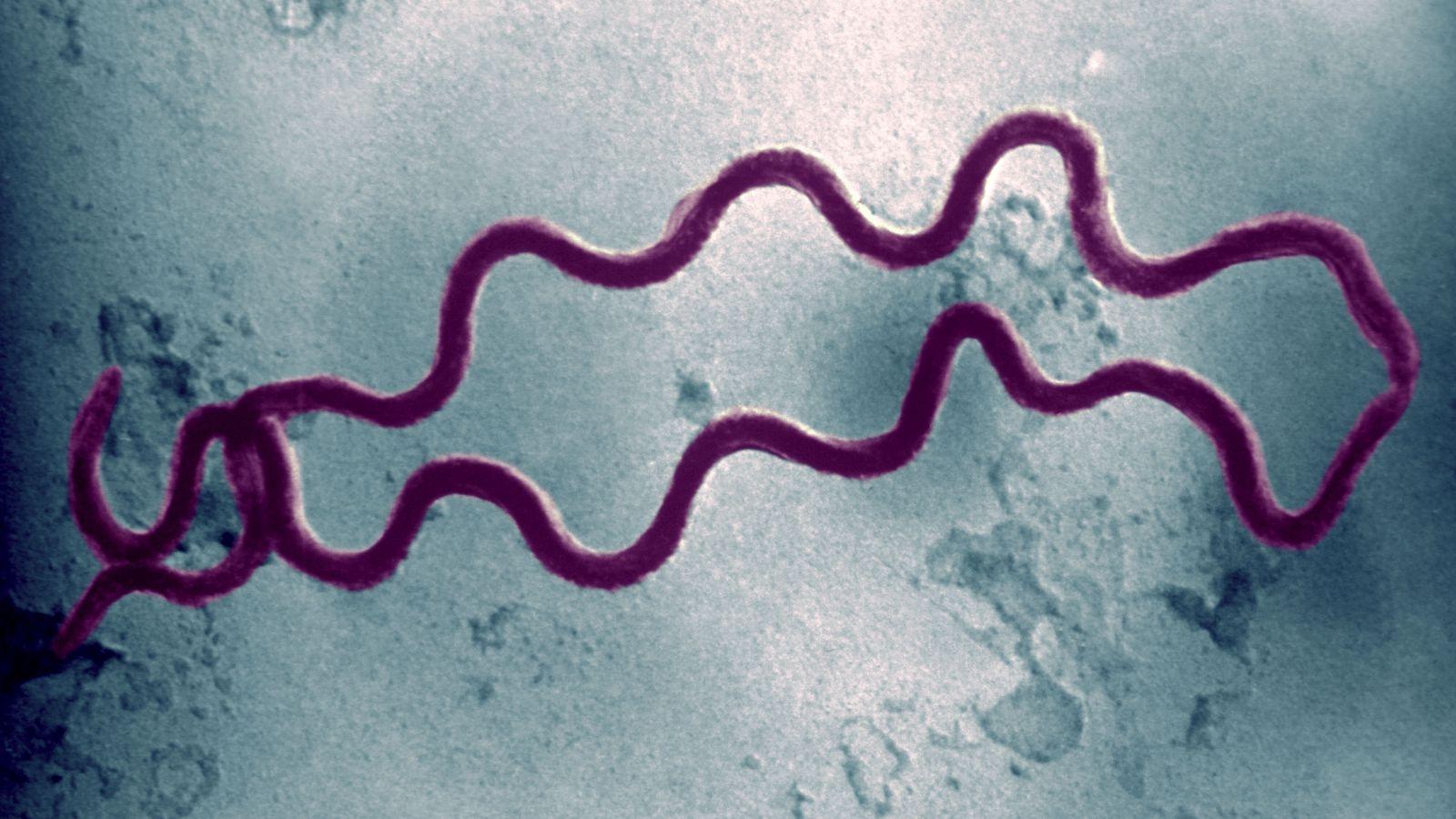
Вероятно, найдено «секретное оружие» вызывающей сифилис бактерии — бледной трепонемы (Treponema pallidum), а именно ген, необходимый для обмана иммунной системы.
Материалы исследования, проведённого в Медицинской школе Вашингтонского университета (UW Medicine) в Сиэтле, опубликованы в журнале PLOS Neglected Tropical Diseases.
Открытие может помочь объяснить, как сифилису удаётся скрываться от иммунной системы на протяжении десятилетий. Это же свойство объясняет способность бактерии повторно заражать ранее инфицированных и вылеченных людей.
Сифилис по-прежнему поддается лечению антибиотиками. Но бледная трепонема приспосабливается, и проблема антибиотикорезистентности становится всё более заметной. Болезнь не отступает и, например, в США показатели инфицирования в последние два десятилетия увеличивались неуклонно. В 2018 году число новых случаев заражения в США увеличилось до более чем 115.000.
По оценкам, в мире происходит 6 миллионов новых случаев заражения сифилисом среди взрослого населения. Эта инфекция ежегодно приводит к приблизительно 300.000 случаям смерти плода и новорождённого.
Биология же Treponema pallidum изучена плохо.
До недавнего времени трепонему не удавалось выращивать в лабораторных условиях. Как следствие, многие обычные методы изучения бактерий не применялись к возбудителю сифилиса.
В ходе исследования учёные сравнили геномы бактерий сифилиса, собранных у человека, который заражался четыре раза. Образцы были получены из крови во время двух инфекций, которые произошли с разницей в шесть лет (а между этими инфекциями человек заражался и лечился ещё дважды).
Исследователи хотели выяснить, есть ли различия между геномами бактерий первой и последней инфекции. Эти различия могли бы показать, как изменились гены бактерий и как эти изменения помогли бактериям заразить человека, чья иммунная система уже встречала несколько различных штаммов сифилиса и должна была, по идее, сформировать иммунный ответ.
Было замечено, что между геномами двух разных образцов было очень мало изменений-за исключением одного гена.
«В общей сложности около 1,1 миллиона оснований, составляющих геном бактерий, претерпели около 20 изменений. Это очень мало, — рассказывает руководитель проекта, доктор Алекс Гренингер (Alex Greninger). — Но в одном этом гене мы увидели сотни изменений».
Ген Treponema pallidum repeat gene K (TprK) представляет собой инструкцию для синтеза белка, обнаруженного на поверхности бактерии. Белки на поверхности бактерии, как правило, хорошо видны иммунным клеткам и поэтому часто становятся основными мишенями иммунной атаки.
Ранее было показано, что TprK служит для конверсии генов — замены одной последовательности ДНК на гомологичную.
Бактериальные клетки с новыми вариантами TprK могут уклоняться от иммунного ответа, что вызывает персистирующую инфекцию.
Персистенция — способность микроорганизмов, которые вызывают инфекцию, долго пребывать в организме человека без проявления клинических симптомов. При этом они способны к активации при определённых условиях.
Замены изменяют облик белка на поверхности микроорганизма, что позволяет ему ускользать от иммунной системы.
Хотя бактерии, вирусы и паразиты могут иметь много белков на поверхности, которые иммунная система могла бы обнаружить и атаковать, во многих случаях только один белок привлекает большую часть внимания. Такие белки называются иммунодоминантами.
«Они могут защитить бактерию, привлекая внимание иммунной системы, — говорит Гренингер. — Белок действует как фактор, отвлекающий иммунную систему от белков, которые могут быть ахиллесовой пятой бактерии. Потребуется дополнительная работа, чтобы определить, имеет ли это место в данном случае».
Гренингер надеется, что полученные результаты помогут исследователям разработать вакцины, которые позволят иммунной системе либо атаковать TprK более эффективно, либо игнорировать TprK и нацеливаться на другие, менее изменчивые белки трепонемы.
Подготовка материала: Сергей Сыров