Американские исследователи сообщили об успехе II фазы испытаний таргетной терапии папиллярной краниофарингиомы ингибиторами сигнального пути B-Raf/MEK. За время испытаний опухоли пациентов уменьшились в размерах на 91 процент.
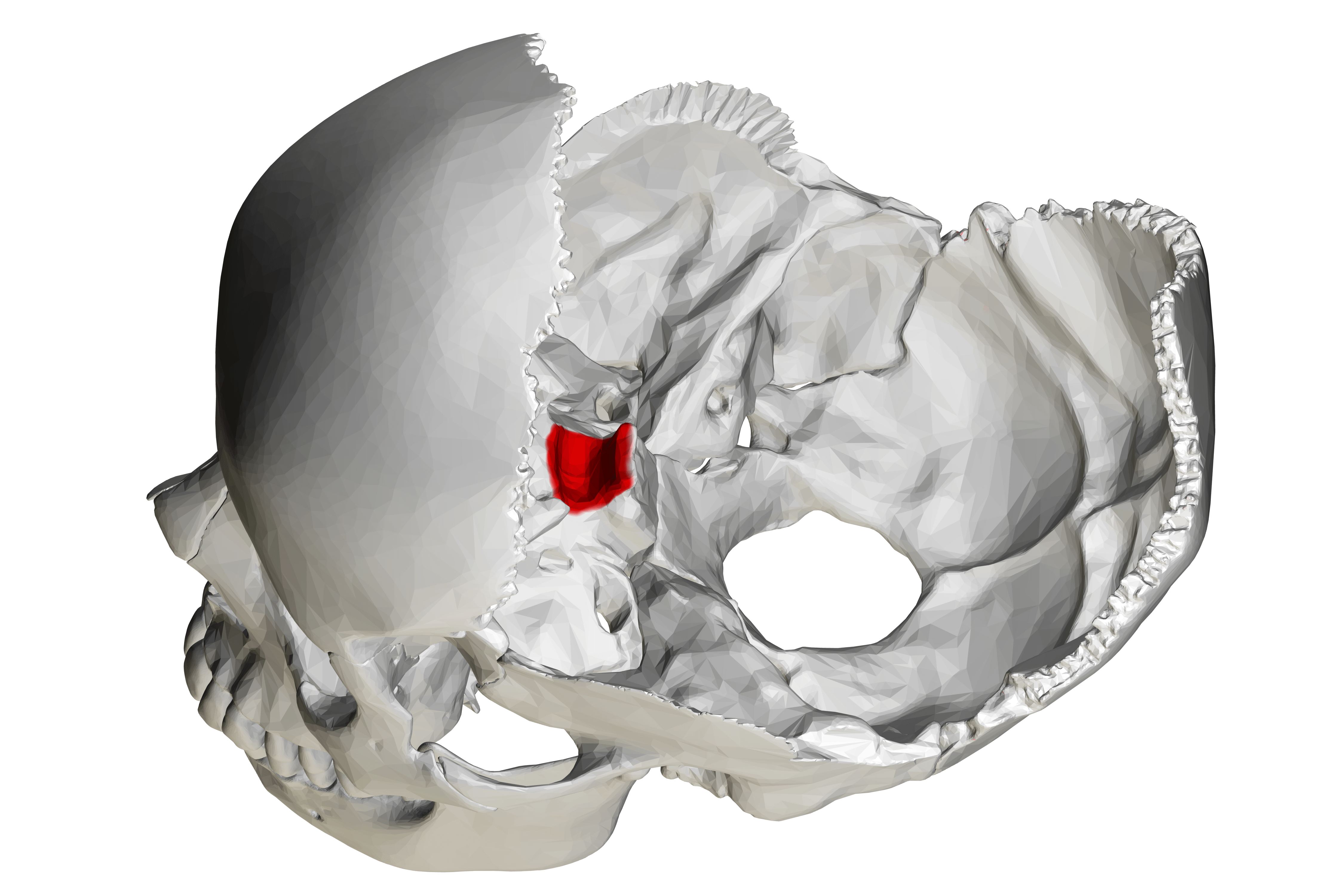
Краниофарингиомы представляют собой доброкачественные, но агрессивно растущие и опасные опухоли, развивающиеся из эмбриональной ткани в области турецкого седла клиновидной кости черепа. В нем расположен гипофиз — придаток мозга, который служит центральным органом эндокринной системы, управляющим работой остальных желез внутренней секреции. В силу своей локализации краниофарингиомы могут затрагивать работу гипофиза и черепно-мозговых нервов. Обычно их удаляют хирургически и/или облучают, однако зачастую после этого развиваются нарушения зрения, нейроэндокринная дисфункция (пангипопитуитаризм, несахарный диабет), расстройства сна, мышления и памяти.
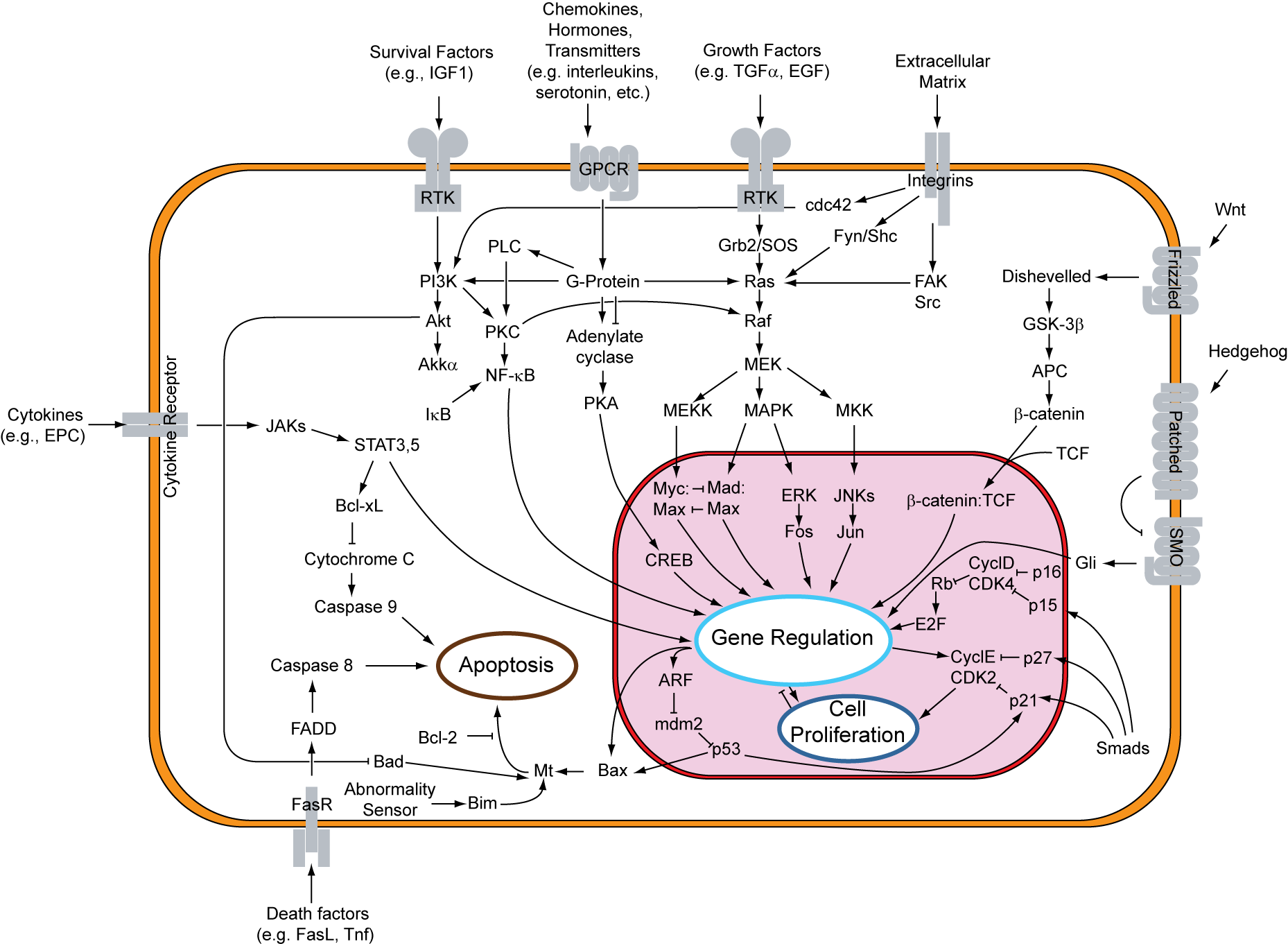
Генотипирование краниофарингиом в недавнее время показало, что более чем у 90 процентов пациентов их клетки содержат мутацию гена BRAF V600E (замена валина на глутаминовую кислоту в 600-м положении). Продукт этого гена — серин-треониновая киназа B-Raf — служит частью внутриклеточного сигнального пути Ras-Raf-MEK-ERK, который играет важную роль в регуляции клеточного цикла и апоптоза; нарушения в нем наблюдаются при многих онкологических заболеваниях. Существуют ингибиторы B-Raf и MEK, разработанные для таргетной терапии меланомы с мутацией BRAF V600E, поэтому возникла идея испытать их у пациентов с папиллярной краниофарингиомой, которая, как выяснилось, носит ту же мутацию.
Присцилла Брастианос (Priscilla Brastianos) из Центра рака Массачусетской больницы общей практики с коллегами по Альянсу клинических испытаний Онкологической сети провели скрининг и отобрали 16 пациентов (медианный возраст 49,5 года) с папиллярной краниофарингиомой и мутацией BRAF V600E, которые не получали лучевой терапии, для участия в открытом мультицентровом исследовании II фазы. Всем им назначали перорально комбинацию 960 миллиграмм ингибитора B-Raf вемурафиниба дважды в день и 60 миллиграмм ингибитора MEK кобиметиниба раз в сутки. Терапию проводили 28-дневными циклами (28 дней вемурафиниба и 21 день кобиметиниба); полный курс состоял из четырех циклов, некоторые пациенты продолжили получать препараты и дальше.
Один пациент прекратил лечение на восьмой день из-за токсических эффектов. У остальных 15 после четырех циклов наблюдался стойкий объективный ответ на терапию. Медианное уменьшение объема опухоли составило 91 процент (от 68 до 99 процентов), медианное время наблюдения — 22 месяца, медианное число циклов — восемь. Выжили без прогрессирования опухоли на 12-й месяц 87 процентов участников, на 24-й месяц — 58 процентов. Прогрессирования опухоли во время приема препаратов не наблюдалось, после его завершения ее рост возобновился у трех пациентов, ни один не умер.
Побочные эффекты, возможно связанные с терапией, наблюдались у 12 участников. Чаще всего встречалась макулопапулярная сыпь (шесть случаев). Наиболее серьезными нежелательными реакциями были гипергликемия и повышение уровня креатинкиназы (по одному случаю). Три пациента прекратили лечение из-за побочных эффектов.
Отчет о работе опубликован в New England Journal of Medicine.
Автор: Олег Лищук