Специалисты Биомедицинского института Нанкина, Института изучения старения Бака и Калифорнийского университета в Беркли обнаружили мутации, которые увеличивают продолжительность жизни более чем в два раза.
Успешные опыты, проведённые на беспозвоночных, планируется повторить с мышами, а впоследствии и с человеком.
Как заявляют авторы открытия, их работа стала результатом развития наиболее передовых исследований генетики и клеточной биологии. Целью проведённых экспериментов являлись гены, отвечающие за работу сигнальных путей − определённых специфических каскадных реакций молекул в клетках.
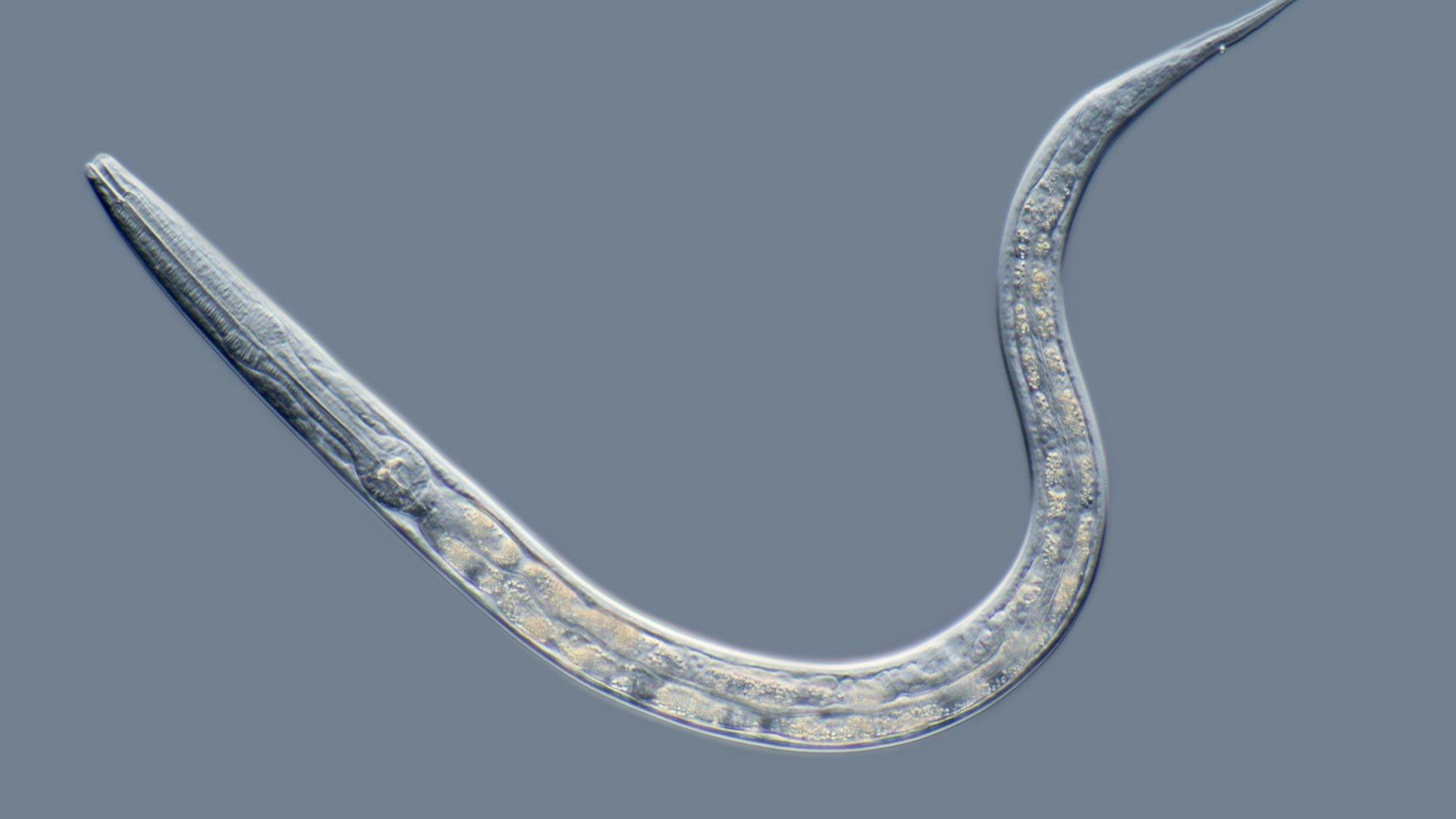
Подопытными-долгожителями стали круглые черви вида Caenorhabditis elegans. Эти крошечные беспозвоночные в длину не превышающие миллиметра не зря называются модельными: организм червей неоднократно выступал в качестве полигона для опытов. Так, недавно на примере C. elegans был показан процесс наступления смерти.
В пресс-релизе института изучения старения Бака написано, что мутации в гене RSKS-1, который отвечает за сигнальный путь питательных веществ, а также гене Daf-2 ─ инсулиновый сигнальный путь, приводят к позитивным изменениям в репродуктивных клетках подопытных.
«В зародышевой линии червей, состоящей из репродуктивных клеток, проявились результаты синергии нескольких мутаций», ─ объясняет Ди Чен (Di Chen) из Биомедицинского института Нанкина.
По словам профессора Панкаж Капахи (Pankaj Kapahi), руководителя исследования, изменение в гене RSKS-1 способствует увеличению продолжительности жизни на 30%, а в гене Daf-2 − на 100%.
«Только на мутации в этих двух генах приходится 130% положительного эффекта суммарно, однако по нашим наблюдениям предельный возраст C. elegans соответствует 400-500 человеческим годам», ─ говорит учёный.
Доктор Капахи рассказывает, что применённая комбинаторная терапия напоминает методики, используемые при борьбе с вирусом иммунодефицита и рака.
«В прежние годы исследование раковых заболеваний было сосредоточено на мутациях в единичном гене, однако впоследствии стало очевидно, что такие патологические процессы управляются целыми классами генов», ─ объясняет Панкаж Капахи.
Следующим шагом будут эксперименты с млекопитающими, а именно мышами. Планируется искусственно вывести генетически модифицированный вид грызунов с врождённым подавлением инсулинового сигнального пути, а затем использовать рапамицин для воздействия на «питательные» сигналы клетки.
Статья авторов исследования опубликована в научном журнале Cell Reports.
Автор: Евгений Парамонов