В 2006 году на международном научном симпозиуме, посвященном синдрому Дауна, была учреждена особая дата — Всемирный день людей с синдромом Дауна. Так как его причиной является трисомия по 21 хромосоме, событие приурочили к двадцать первому дню третьего месяца.
Мы решили разобраться, далеко ли продвинулась медицина в понимании механизма развития симптомов этого синдрома, и можно ли будет в будущем добиться его полного излечения.
Что это за болезнь?
Ученые не зря проявляют повышенный интерес к изучению синдрома Дауна — это заболевание, обусловленное появлением у эмбриона лишней копии 21 хромосомы (как правило, случайным), встречается довольно часто. В 2015 году в мире насчитывалось более пяти миллионов людей с этим диагнозом. Вероятность рождения ребенка с такой хромосомной аномалией увеличивается с 0,1 процента у 20-летних женщин до трех процентов у женщин в возрасте 45 лет. Но большинство больных детей рождается у матерей моложе 35 лет — потому, что пик деторождения приходится на этот возраст. Кроме того, вероятность появления лишних копий хромосом или их фрагментов увеличивается с возрастом и у мужчин, так что отец тоже может внести свой вклад в рождение больного ребенка.
Лишняя хромосома создает множество опасностей для здоровья. По данным Департамента здравоохранения США, половина детей с трисомией по 21 хромосоме страдает врожденным пороком сердца, который требует хирургического вмешательства сразу после рождения. Кроме того, люди с синдромом испытывают проблемы со зрением, включая частое развитие катаракты, в 70 процентах случаев у них развиваются нарушения слуха. Ослабленный иммунитет и подверженность инфекциям сочетаются с повышенным на порядок риском развития лейкозов.
Мышечная слабость, проблемы с позвоночником, расстройства сна, заболевания пищеварительного тракта, снижение функций щитовидной железы — вот неполный список возможных (но необязательных) обстоятельств, с которым могут столкнуться носители лишней копии 21 хромосомы. Одной из важных проблем детей с синдромом Дауна является задержка умственного развития. С возрастом у таких людей значительно повышается риск развития болезни Альцгеймера. Тем не менее, прогресс в медицине привел к тому, что в развитых странах продолжительность жизни людей с этим синдромом в настоящее время составляет 50-60 лет, причем многие из них социально адаптированы и являются полноценными членами общества. Так как большинство сопутствующих медицинских симптомов теперь можно устранить поддерживающей терапией, основной проблемой таких людей остается социальная стигма. Общество оказывает колоссальное давление на матерей таких детей, а возможности для реабилитации и социализации доступны далеко не всем.
История синдрома
Характерные для синдрома Дауна фенотипические черты были обнаружены на лицах статуэток, сделанных 2,5 тысячи лет назад, и это означает, что трисомия не является приметой нашего времени. Трисомия по 21 хромосоме была названа синдромом Дауна в честь врача Джона Дауна, который впервые составил ее клиническое описание в 1866 году (сам Даун, впрочем, назвал синдром «монголизмом» — из-за характерной для больных раскосости глаз). Тем не менее, генетическая причина синдрома была обнаружена французскими учеными только в 1959 году.
Это открытие заставило врачей сформулировать гипотезу «увеличения дозы генов», которая была частично подтверждена биохимическими анализами. Она подразумевает, что нарушения возникают из-за избытка некоторых белков, которые продуцируются с нормальных генов на лишней хромосоме. К «избыточным» были отнесены ферменты окислительно-восстановительного метаболизма, метаболизма углеводов и некоторых кофакторов. Исходя из этого, некоторые исследователи предложили лечить синдром витаминно-минеральными комплексами. В 1960-х годах доктор Генри Теркел (Henry Turkel) утверждал, что разработал комплекс из 48 веществ. Он в течение многих лет давал его своим пациентам, и он, якобы, восстанавливал их интеллектуальные способности. Впоследствии врачи заявляли о пользе терапии на основе витаминов, минералов и тироидного гормона, антиоксидантов и фолиевой кислоты. Тем не менее, никаких клинических испытаний в то время не проводили, и документальных подтверждений эффективности этих комплексов не существует.
Откуда берутся все эти симптомы?
21 хромосома человека (HSA21) — самая маленькая аутосома (неполовая хромосома), тем не менее, она содержит порядка 400 генов, 250 из которых кодируют белки. Исследование экспрессии генов в клеточных линиях с лишней копией HSA21 показало, что только около трети генов, содержащихся на ней, экспрессируются на избыточном уровне. При этом увеличение экспрессии большей части из них отражает увеличение копийности хромосомы (то есть возрастает в полтора раза), а экспрессия семи процентов увеличена более значительно. Именно среди этой порции генов ученые искали причины развития болезненных симптомов.
Некоторые гены, попавшие в эту группу, могут быть ответственны за нарушение синтеза и репарации ДНК. Ген COL6A1, необходимый для синтеза определенного типа коллагена, может быть связан с развитием миопатии и нарушений работы сердца. Сверхэкспрессия гена CRYA1, кодирующего один из белков-кристаллинов, формирующих хрусталик, может провоцировать катаракту. Увеличение количества тирозинкиназы, кодируемой геном DYRK1A, и экспрессирующейся в мозге, вероятно, препятствует развитию нервной системы. Оказалось, что большое количество «подозреваемых» сосредоточено в одном большом локусе, который назвали «основным участком, ответственным за развитие синдрома Дауна» (DSCR — Down Syndrome critical region). Тем не менее, для большинства этих генов участие в развитии симптомов заболевания экспериментально не доказано.
С развитием генной инженерии, в изучении большого количества генетически обусловленных заболеваний на помощь ученым приходят мышиные модели. Несмотря на то, что мышиные аналоги генов 21 хромосомы человека разбросаны по трем разным хромосомам, исследователям удалось продублировать большие участки, содержащие десятки нужных генов, и получить линии животных, демонстрирующие «человеческие» симптомы синдрома Дауна. Мыши линии Ts65Dn на сегодняшний день представляют одну из самых популярных моделей исследования этого синдрома. В частности, на этой линии удалось доказать, что в раннем развитии болезни Альцгеймера при синдроме Дауна виновата повышенная экспрессия гена APP, кодирующего предшественник амилоидного белка.
А можно ли это лечить?
На сегодняшний день общепринятой терапии для синдрома Дауна не существует, однако прорабатывается целый ряд подходов. Помимо симптоматического лечения сопутствующих расстройств, таких как порок сердца и нарушение работы щитовидной железы, усилия ученых направлены на поиск препаратов, помогающих восстановить интеллектуальные функции людей с синдромом Дауна. При поиске перспективной терапии первыми подопытными становятся вышеупомянутые мыши.
Умеренное положительное воздействие на обучаемость и память было обнаружено при имплантации модельным мышам в мозг стволовых клеток-предшественников нейронов. Однако говорить о применении на людях этого метода пока преждевременно. Сюда же относится и генотерапия, например, подавление экспрессии упомянутого гена DYRK1A при помощи РНК-интерференции. Этот подход также дал значимые результаты на мышах. Однако подавить активность продукта DYRK1A можно и более простым способом — его природным ингибитором является галлат эпигаллокатехина (EGCG), который в больших количествах содержится, например, в чае.
Множество исследований было посвящено восстановлению функций мозга при помощи воздействия на количество нейромедиаторов, например, гамма-аминомасляной кислоты и серотонина. В испытаниях на животных хорошо себя проявили соли лития, которые ранее использовали для лечения биполярного расстройства. Одним из ярко выраженных биохимических нарушений, сопровождающих практически все ткани больных синдромом Дауна, является окислительный стресс. Эксперименты на мышах показали, что прием антиоксидантов, в частности, витамина Е, нормализует количество нейронов и улучшает рабочую и пространственную память животных.
Самая простая терапия, которая предвещает минимум побочных эффектов — это физическая активность и обогащенная стимулами окружающая среда. На мышах было доказано, что эти условия увеличивают нейрогенез и формирование синапсов, которые и являются показателями развития мозга.
К настоящему времени ряд молекул был проверен и на людях (преимущественно детях и подростках) в проведенных по современным стандартам клинических испытаниях. Ученые оценили эффективность ингибиторов ацетилхолинэстеразы, которые применяются в терапии болезней Альцгеймера и Паркинсона (ривастигмина и донепезила), популярного ноотропа пирацетама, фолиевой кислоты, витамина Е, гормона роста, антагониста глутаматных рецепторов мемантина и компонента чая EGCG. К сожалению, практически все эти препараты никак не улучшили интеллектуальные показатели больных, оцениваемые по специальным тестам. Исключение составил только эпигаллокатехин — небольшое предварительное исследование показало улучшение памяти у детей в результате приема вещества в течение некоторого времени. Вероятно, эта молекула не является безнадежной, и оптимизация протоколов лечения может со временем дать свои плоды.
Несмотря на провальные испытания большинства кандидатов, ученые предполагают, что лечение может быть эффективным, если его начинать еще в утробе матери, в то время, когда мозг еще только развивается. Эта гипотеза снова оправдала себя на мышах, однако до испытаний на беременных женщинах исследователи пока не добрались.
А можно ли просто выключить лишнюю хромосому?
Самые радикальные способы лечения синдрома Дауна и других хромосомных нарушений предлагает генная инженерия. Современные биохимические инструменты позволяют как «выключать» лишние гены, так и вставлять новые почти в любое место генома.
Например, исследователи из университета Вашингтона смогли избавиться от лишней хромосомы в клетках при помощи популярного у генетиков метода позитивно-негативной селекции. Для этого в хромосому при помощи вирусного вектора сначала вставили кассету, содержащую ген устойчивости к антибиотику и ген фермента синтеза нуклеотидов. На первом этапе ген устойчивости к антибиотику помог отобрать нужные клетки с интегрированной в геном кассетой (позитивная селекция). На втором этапе в ростовую среду к клеткам добавили вещество — предшественник нуклеотидов. Встроенный в клетки фермент превращал его в токсичное вещество, в результате чего клетки, содержащие кассету, погибали — или выбрасывали лишнюю хромосому (негативная селекция).
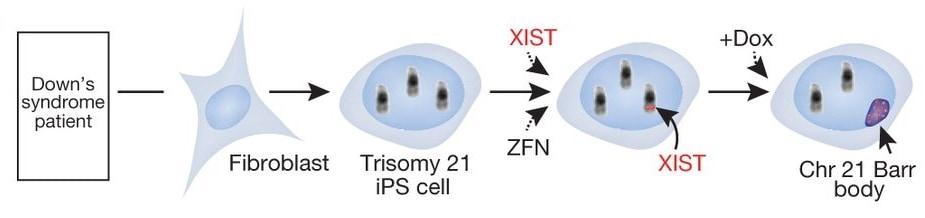
Другая группа американских ученых предложила более изящное решение для инактивации лишней хромосомы. Исследователи провели аналогию с природным механизмом выключения Х-хромосомы. У женщин в клетках две Х-хромосомы, но работает из них только одна, а другая инактивируется с образованием компактного «клубочка» из ДНК и белков, называемого тельцем Барра. Происходит это с участием гена XIST, с которого считывается длинная некодирующая молекула РНК, обеспечивающая подавление активности всех генов на Х-хромосоме. Исследователи вставили ген XIST при помощи инструмента редактирования генома — распознающей определенную последовательность ДНК нуклеазы — в локус уже известного нам гена DYRK1A. Активность гена XIST привела к тому, что лишняя 21 хромосома «свернулась в клубочек» и образовала неактивное тельце Барра.
Китайские ученые предложили использовать для уничтожения лишних хромосом технологию CRISPR-Cas9. Для этого в клетки ввели коктейль из направляющих РНК — «затравок» для нуклеазы Cas9, указывающих, где ему резать, и сам Cas9. В результате узнавания множества сайтов белок «покрошил» хромосому на кусочки. Таким образом исследователям удалось с высокой эффективностью избавиться от Y-хромосомы, и с эффективностью порядка 15 процентов — от лишних аутосом, включая седьмую, 14 и 21 хромосомы.
Увы, генные инженеры пока не добрались даже до мышей — все упомянутые эксперименты выполнены на стволовых клетках. Кроме того, методы исправления генома «больных» клеток оставляют вопросы: как «направить» средство редактирования к одной копии хромосомы, в то время как в клетке их три? Что, если интеграция окажется слишком эффективной, и вместо одной выключатся две хромосомы? Даже если мы все-таки захотим применить методы редактирования ДНК к человеку, как обеспечить доставку инструментов во все клетки?
Пока энтузиасты генной инженерии человека предлагают исправлять мутации еще на стадии эмбриона, однако хромосомные нарушения, как правило, не являются наследственными заболеваниями. Если родители захотят зачать ребенка «в пробирке», что в любом случае требуется для редактирования генома, проще будет отобрать здоровый эмбрион еще на стадии оплодотворения.
Таким образом, генная инженерия тоже не обещает перспектив полного излечения людей с синдромом Дауна. Однако одну вполне реализуемую вещь она способна предложить. Как было упомянуто в начале статьи, больные синдромом Дауна в высокой степени подвержены риску развития лейкемии. В то же время, исследователи, которые занимаются иммунотерапией рака, уже научились заменять у пациентов «больные» иммунные клетки на генетически модифицированные (об этом можно прочитать здесь). Таким образом, если взять у человека с синдромом Дауна иммунные клетки, выключить в них лишнюю хромосому и вернуть клетки обратно, одной потенциальной проблемой со здоровьем у человека будет меньше.
Лечить, предотвратить или смириться?
Пока вылечить синдром Дауна не представляется возможным, медицина предоставляет будущим матерям другую возможность — проверить, не является ли плод носителем лишней хромосомы, еще в утробе. Для этого используется пренатальная диагностика, которая делается на разных стадиях беременности. «Традиционные» методы включают в себя ультразвуковую диагностику, определение концентрации набора белковых маркеров в сыворотке крови матери, исследование околоплодных вод или тканей плаценты. Их точность составляет около 80-90 процентов. Самой лучшей диагностикой на сегодняшний день является секвенирование циркулирующей ДНК плода в крови матери. Точность этого метода превышает 99 процентов, к тому же метод является неинвазивным, а значит, наиболее безопасным как для матери, так и для ребенка.
Пренатальная диагностика хромосомных заболеваний, при всей своей надежности и простоте, несет этическую составляющую, ведь за постановкой диагноза более чем в 90 процентов случаев следует прерывание беременности. В то время как большинство медиков убеждены, что это правильный выбор, некоторые специалисты называют такое положение вещей «современной евгеникой».
Притом, что на воспитание ребенка с синдромом Дауна родители тратят гораздо больше ресурсов, чем на воспитание «обычного» ребенка, их усилия часто окупаются. Учитывая, что большинство сопутствующих синдрому заболеваний можно устранить вспомогательной терапией, основной проблемой в социализации таких людей остается интеллектуальное развитие. Тем не менее, в большинстве случаев дети с синдромом Дауна обучаемы, при применении специальных развивающих методик дети превращаются в полноценных членов общества, не являющихся обузой для него. Некоторые люди с этим синдромом закончили университет, являются успешными актерами или музыкантами. Среди них, например, Карен Гаффни — руководитель некоммерческой организации помощи детям с с ограниченными возможностями, или музыканты финской панк-рок группы Pertti Kurikan Nimipäivät (PKN).
Небольшой опрос среди ста семей, проведенный канадским Обществом синдрома Дауна в Британской Колумбии, показал, что только 40 процентов родителей хотели бы вылечить своего ребенка от синдрома, если бы лекарство существовало. 27 процентов родителей сказали, что они не стали бы лечить ребенка — они любят его таким, какой он есть. Это лишний раз напоминает о том, что «люди всякие нужны, люди всякие важны», и при поддержке окружающих каждый может найти свое место под солнцем.
Автор: Дарья Спасская