Мы не устаем говорить о том, как велика роль биологических часов в нашей жизни: от них зависит наш сон, они влияют на иммунитет, на обмен веществ, на работу сердца и т. д. и т. п.

И если спустится на несколько уровней ниже, к нуклеиновым кислотам и белкам, то мы увидим, что суточным ритмам подчиняются даже главные молекулярные процессы, без которых не может обойтись ни одна клетка.
Азиз Санджар и его коллеги из Университета Северной Каролины в Чапел-Хилл описывают в своей статье в PNAS взаимосвязь биологических часов и репарации ДНК. Возможно, многие помнят, что Санджар был одним из трех лауреатов Нобелевской премии по химии 2015 года – тогда ее дали как раз за ДНК-репарацию, точнее, за расшифровку молекулярных механизмов, с помощью которых клетка исправляет дефекты в ДНК.
Хотя ДНК, как мы знаем, молекула чрезвычайно прочная и стабильная, в ней все равно регулярно случаются мутации: цепи ДНК рвутся, а на месте правильных генетических букв появляются другие, неправильные. Поэтому механизмы репарации очень важны, и поэтому они работают почти без остановки.
Но, как оказалось, активность ДНК-ремонтных машин зависит от времени суток. Исследователи экспериментировали с цисплатином – особым соединением платины, которое, соединяясь с ДНК, портит ее структуру: из-за цисплатина возникают прочные химические связи (сшивки) как между цепями, так и внутри одной цепи ДНК.
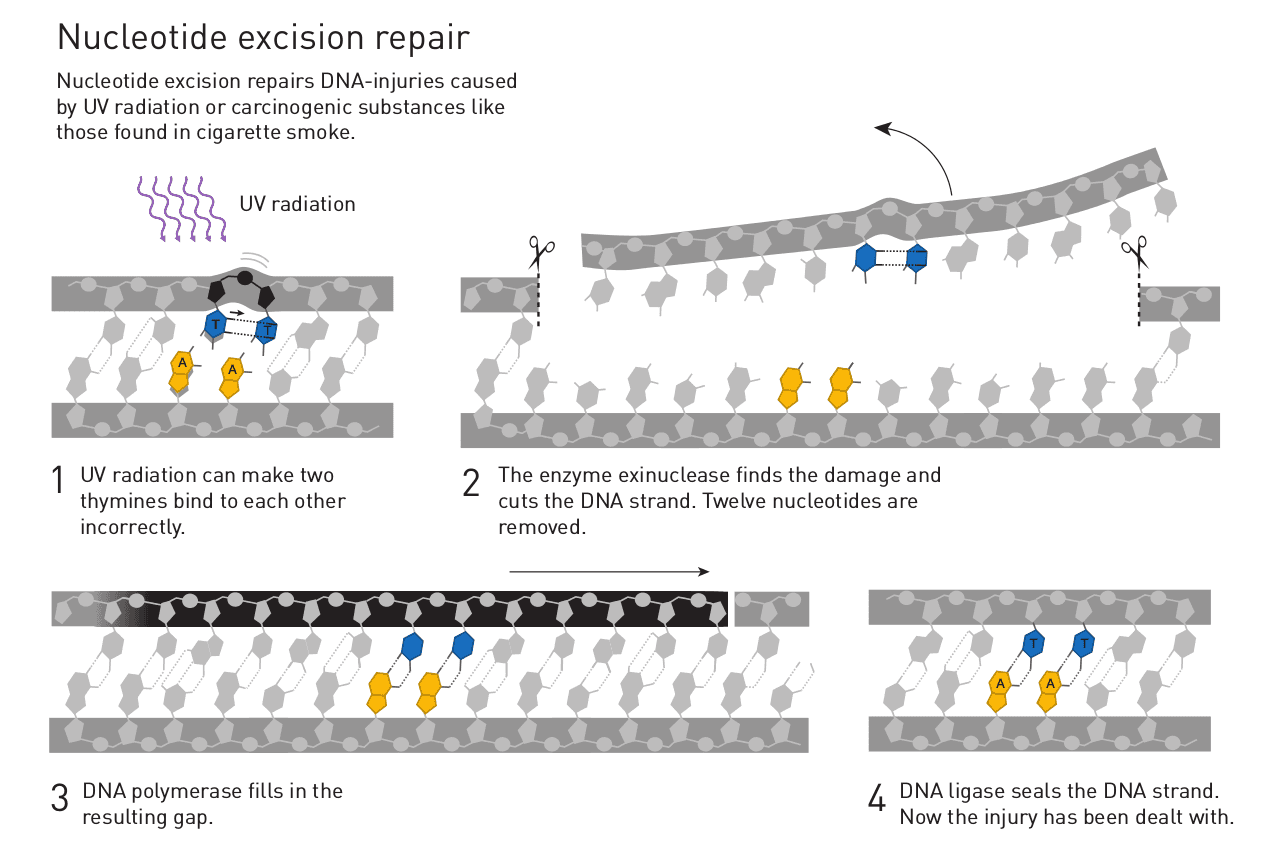
Напомним, что обе цепи в двухцепочечной молекуле ДНК в норме соединены друг с другом водородными связями, которые достаточно легко разорвать. А разрывать связи между цепями приходится часто: молекулярные машины, которые читают генетическую информацию, могут делать это, только если цепи ДНК разъединены. Из-за появляющихся жестких, неразрываемых связей между цепями ДНК у клетки начинаются проблемы: она не может ни белки синтезировать, ни делиться.
Чтобы синтезировать белок, нужно сначала снять с гена копию в виде молекулы матричной РНК, а уже потом на матричной РНК белоксинтезирующие машины будут собирать полипептидную цепь белка. Но чтобы сделать копию РНК, нужно разделить двуспиральную ДНК, и тогда специальные транскрибирующие белки (транскрипцией называют синтез РНК на ДНК-шаблоне) смогут собрать молекулу РНК.
Если же клетка хочет делиться, то для начала ей нужно провести репликацию, то есть сделать новые копии ДНК, а чтобы синтезировать новые ДНК, нужно опять-таки разделить цепи старой. Если же возникли прочные сшивки внутри одной цепи, то опять все плохо: с такими нуклеотидами (генетическими буквами) ферменты репликации и транскрипции опять же не могут работать.
Подопытным мышам давали цисплатин в течение 24 часов, одновременно отслеживая, в каких местах генома системы репарации ДНК будут исправлять цисплатиновые дефекты. В итоге удалось найти почти 2000 генов, на которых репарирующие ферменты работали по-разному в разное время суток, притом с некоторыми особенностями.
Мы только что сказали, что когда на гене синтезируется РНК-копия, двуцепочечная ДНК расплетается – но только одна из ее цепей служит шаблоном для синтеза РНК. Так вот, если речь идет о той цепи, с которой снимают копию РНК, то такие цепи клетка активнее всего ремонтирует перед рассветом или перед закатом, в зависимости от конкретного гена.
А вот другой, нетранскрибируемой цепью, ремонтные машины занимаются перед закатом, независимо от того, какой это ген. Стоит уточнить, что и в остальное время репарация ДНК тоже идет, просто в некоторые часы она становится особенно активной, и такие периоды активности, как оказалось, явно подчиняются суточным ритмам.
О том, как работают биологические часы мы, неоднократно рассказывали (кстати говоря, за молекулярный механизм биологических часов тоже дали Нобелевскую премию – в прошлом году). Очевидно, что физиологические изменения, соответствующие суточным ритмам, не могли бы происходить, если бы не было суточных изменений в соответствующих генах, и действительно, сейчас мы знаем уже очень много генов, которые активизируются по часам. Можно предположить, активность репарирующих систем подчинена расписанию тех генов, которые они ремонтируют; впрочем, без дополнительных экспериментов какие-либо далеко идущие выводы тут делать рано.
И, конечно, здесь нельзя не отметить чрезвычайно большое практическое значение полученных результатов. Возможно, кто-то отметил про себя, что авторы работы использовали в своих экспериментах вещество, которое используют против злокачественных опухолей.
Цисплатином действительно можно убивать самые разные раковые клетки – из-за тех дефектов в ДНК, которые он вызывает, они не могут ни делиться, ни вообще вести хоть какую-то активную жизнь. Проблема, однако, в том, что и обычные клетки чрезвычайно страдают от цисплатина, и особенно сильно от него страдают печень, почки и нервная система. Возможно, что здоровые ткани можно как-то защитить от него, если применять терапию с учетом суточных особенностей в ДНК-репарирующих системах; возможно, что его действие на раковые клетки можно усилить, если отключить биологические часы в опухолях. Возможно, что такой подход можно использовать не только в случае с цисплатином, но и с другими методами терапии, и не только с раком, но и с другими заболеваниями.
На самом деле, медики сейчас все активней занимаются хронобиологией, однако, по словам самого Азиза Санджара, до сих пор большинство работ в этой области останавливались только на внешних проявлениях суточных ритмов: больной получал лекарство, и в зависимости от времени суток у него отмечали более или менее сильное улучшение; механизм же феномена оставался за кадром. Но чтобы в полной мере извлечь медицинскую пользу из наших биологических часов, нужно знать во всех молекулярных деталях их механизм, и как раз исследования, подобные вышеописанному, нас к этому и приближают.
Автор: Кирилл Стасевич