Исследователям из Университета Кюсю удалось с помощью стволовых клеток мыши воссоздать структуры яичника, необходимые для формирования зрелых яйцеклеток. Более того, они смогли применить свои результаты для создания функциональных яйцеклеток и даже вырастить жизнеспособных мышей.
Работа опубликована в журнале Science. Команда надеется, что полученные результаты приближают нас к лечению женского бесплодия путём понимания его глубинных причин, а также послужат делу сохранения видов животных, находящихся под угрозой исчезновения, — путём производства яйцеклеток.
В изучении стволовых клеток особенно важно понимание того, как одна клетка, способная стать чем угодно, может превращаться в клетки, составляющие орган или ткань, — этот процесс называется «дифференциацией». Кацухико Хаяши (Katsuhiko Hayashi), профессор факультета медицинских наук Университета Кюсю, работает над раскрытием механизмов, лежащих в основе роста и развития фундаментальной клетки жизни — яйцеклетки.
Ооцит — это незрелая стадия яйцеклетки. В понимании развития ооцитов было сделано много важных открытий, вплоть до создания мышиных и человеческих ооцитов из соответствующих стволовых клеток и даже выведения здоровых мышей. Однако одним из основных препятствий в этом процессе является создание надлежащей системы поддержки, которая помогала бы превращать стволовые клетки в ооциты. В организме первичные ооциты начинают развиваться в период полового созревания при поддержке других клеток. Часть яичника, которая в конечном итоге производит зрелую яйцеклетку, называется фолликулом.
«Хотя мы смогли искусственно создать мышиные ооциты из стволовых клеток, для их созревания мы должны были соединить их с клетками, называемыми гонадальными соматическими клетками, которые были извлечены из мышей. Если мы надеемся лучше понять развитие ооцитов и применить эту технологию к животным, находящимся под угрозой исчезновения, и даже к людям, мы также должны быть в состоянии создать систему поддержки из стволовых клеток»,
Первым шагом команды было изучение мышей и определение критических генов, которые запускают производство гонадальных соматических клеток. После идентификации этих клеток, исследователи тщательно протестировали стволовые клетки мышей в различных условиях, пока не смогли получить из них клетки с похожими характеристиками.
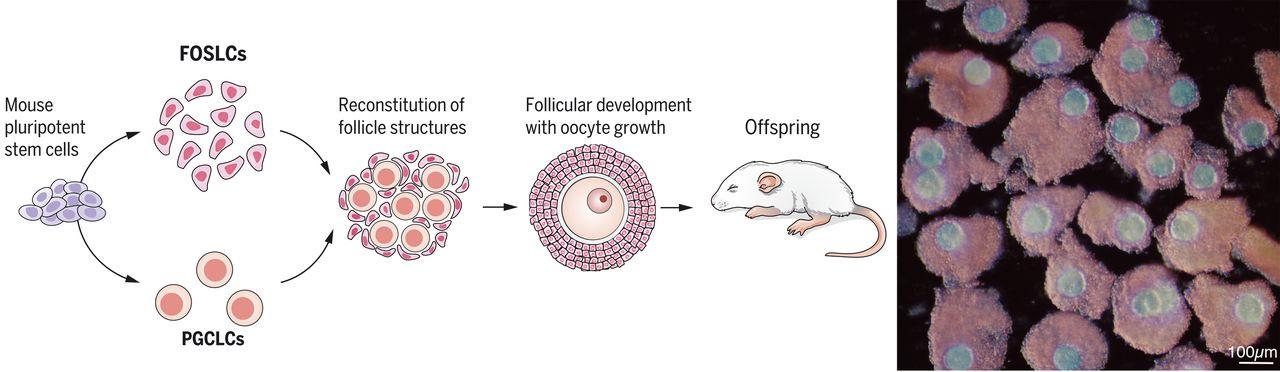
Учёные назвали эти клетки фетальными соматическими клетками яичников, или FOSLC. Следующим шагом было объединение FOSLCs с полученными из стволовых клеток примордиальными зародышевыми клетками — предшественниками ооцитов, получение которых было отработано в ходе предыдущего исследования, и наблюдение за тем, созреют ли они в ооциты.
После нескольких дней роста клетки начали формировать фолликулы, окружающие ооциты. После подтверждения того, что эти клетки на самом деле являются полностью выросшими ооцитами, яйцеклетки были оплодотворены и подсажены самке мыши, сыгравшей роль суррогатной матери. В итоге команда учёных получила выводок здоровых мышат.
Ожидается, что новая система сможет производить большое количество ооцитов без необходимости забора необходимых клеток у животных-хозяев.
«Это значительно поможет улучшить наше понимание развития фолликула яичника и репродуктивной биологии в целом. Применение на людях технически возможно, но из-за генетической и эпигенетической нестабильности гамет, полученных in vitro, мы всё ещё должны тщательно продумать и обсудить этику и технологию такого применения. Мы продолжим нашу работу для дальнейшего выяснения как фундаментальных, так и уникальных механизмов воспроизводства жизни»,
Подготовка материала: Мария Толмачёва