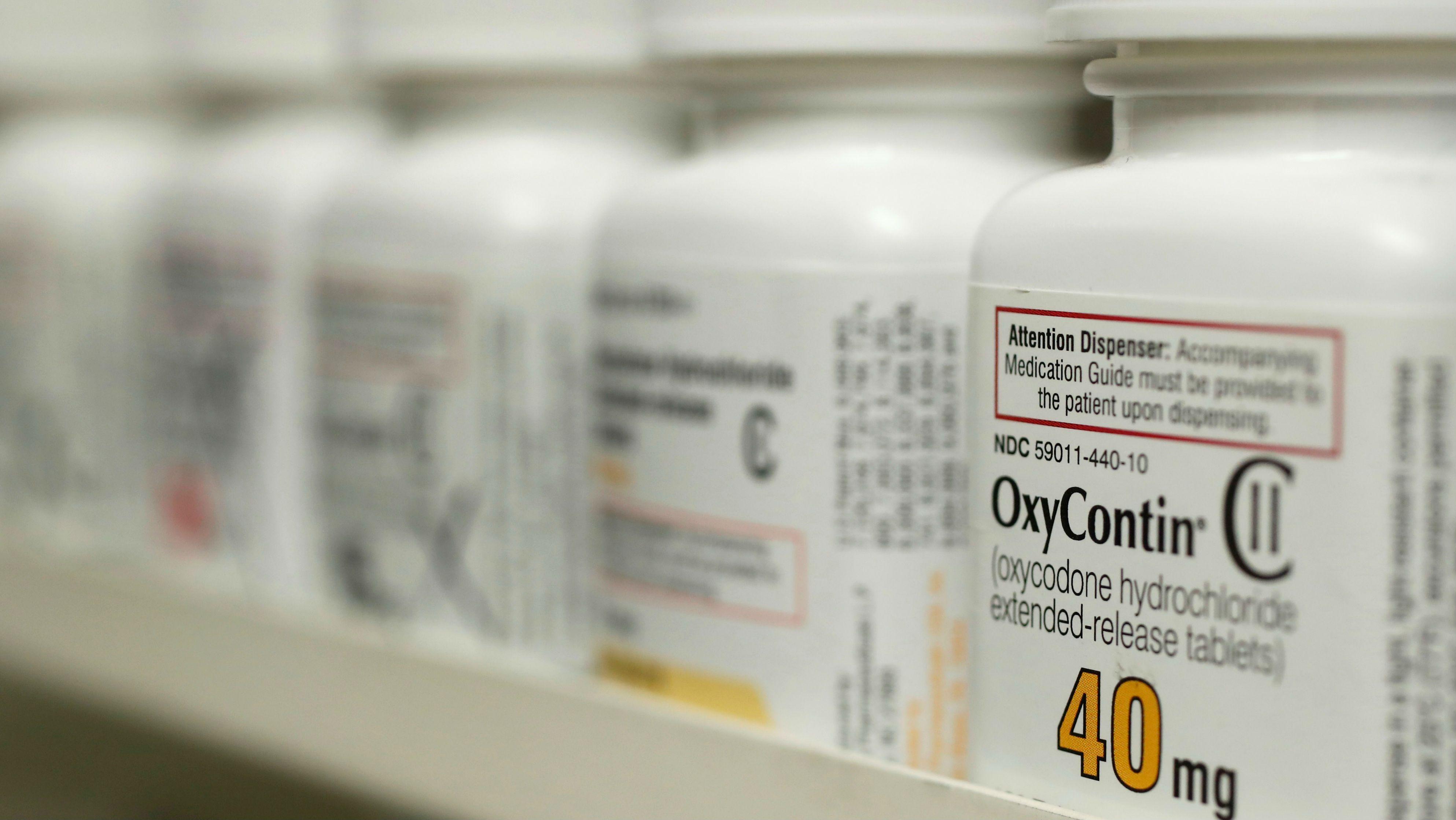
В рамках борьбы с растущей угрозой злоупотребления опиоидными препаратамиFDA выдало распоряжение изъять из продажи опиоидный анальгетик оксиморфон гидрохлорид (oxymorphone hydrochloride) производства компании Endo International Plc.
Как отмечается в заявлении американского регулятора, это первый случай, когда эксперты FDA приняли решение вывести с рынка опиоидный анальгетик во избежание проблем общественного здоровья и здравоохранения, связанных с последствиями злоупотребления препаратом.
Сообщается, что решение FDA основано на анализе доступных данных, продемонстрировавших значительный рост показателей злоупотребления препаратом для внутривенного применения, и следует за заключением консультативного комитета FDA, согласно которому преимущества препарата больше не перевешивают риски. Прием препарата был также связан с серьезной вспышкой ВИЧ-инфекции, гепатита С и развитием тромботической микроангиопатии, говорится в сообщении регулятора.
Как завил руководитель FDA Скотт Готтлиб, столкнувшись с опиоидной эпидемией, мы обязаны предпринять все необходимые шаги для сокращения масштабов некорректного употребления и злоупотребления опиоидами. По его словам, FDA будет продолжать принимать меры по регулированию опиоидных анальгетиков не только в случае, если риски применения препарата перевешивают преимущества, но и в случае риска злоупотребления.
Автор: Нелли Хамзина