Биологи из Германии предложили еще одно объяснение тромбообразования после введения векторных вакцин.
В экспериментах на культуре клеток они доказали, что РНК, образующаяся после транскрипции ДНК из аденовирусного вектора, претерпевает неправильный сплайсинг. Из-за этого спайк-белок презентируется не на поверхности клеток, а выходит из них в свободной форме, связывается с ACE2 рецепторами эндотелия и вызывает аутоиммунные реакции. Исследование опубликовали в eLife.
Через несколько месяцев после начала прививочной кампании у вакцин, которые используют для иммунизации аденовирусный вектор, обнаружили редкий побочный эффект — тромбоз. В апреле 2021 года Европейский медицинский регулятор добавил его в список побочных эффектов вакцины AstraZeneca, а затем — препарата от Johnson & Johnson.
Когда биологи начали изучать, почему именно возникал тромбоз, то они обнаружили, что аденовирус может связываться с тромбоцитарным цитокином PF4. Эти комплексы иммунная система затем распознает как чужеродные и запускает выработку антител против PF4, что приводит к тромбозам.
Альтернативное объяснение того, почему именно возникают тромбы, предложили немецкие ученые во главе с Рольфом Маршалеком (Rolf Marschalek) из Франкфуртского университета имени Гете. По их версии, все дело в том, что аденовирусный вектор доставляет в организм информацию о спайк-белке коронавируса, «записанную» в форме ДНК, а не РНК, как в препаратах от Pfizer и Moderna. Попадая в клетку, ДНК освобождается из вектора и происходит ее транскрипция. Образующаяся в ходе этого процесса РНК затем претерпевает все те же посттранскрипционные изменения, что и любая другая РНК.
Исследователи предположили, что на этом этапе РНК, кодирующая спайк-белок, претерпевает неправильный сплайсинг — ферменты эндонуклеазы разрезают ее в так называемых криптических сайтах. В результате образуется конечная РНК, у которой отсутствуют некоторые составляющие спайк-белка коронавируса.
Сначала биологи проверили свою гипотезу in silico: с помощью онлайн-платформы SpliceRover они нашли возможные места сплайсинга в последовательности, кодирующей спайк-белок SARS-CoV-2 в вакцинах AstraZeneca и Janssen. Ученые обнаружили, что сплайсинг в конечном итоге приводит к образованию спайк-белка, в котором отсутствует трансмембранный якорный белок. Такой спайк-белок выходит из клеток, связывается с рецепторами ACE2 на поверхности клеток эндотелия и запускать аутоиммунные реакции против них с образованием тромбов. При обычном же течении событий после иммунизации векторными вакцинами спайк-белок презентируется на поверхности клеток и не находится в крови в свободной форме.
Исследователи экспериментально показали, что такие продукты сплайсинга действительно образуются — ученые внесли в культуру клеток аденовирусные векторы из вакцин AstraZeneca и Johnson & Johnson, а затем c помощью ПЦР посмотрели на получившиеся продукты сплайсинга.
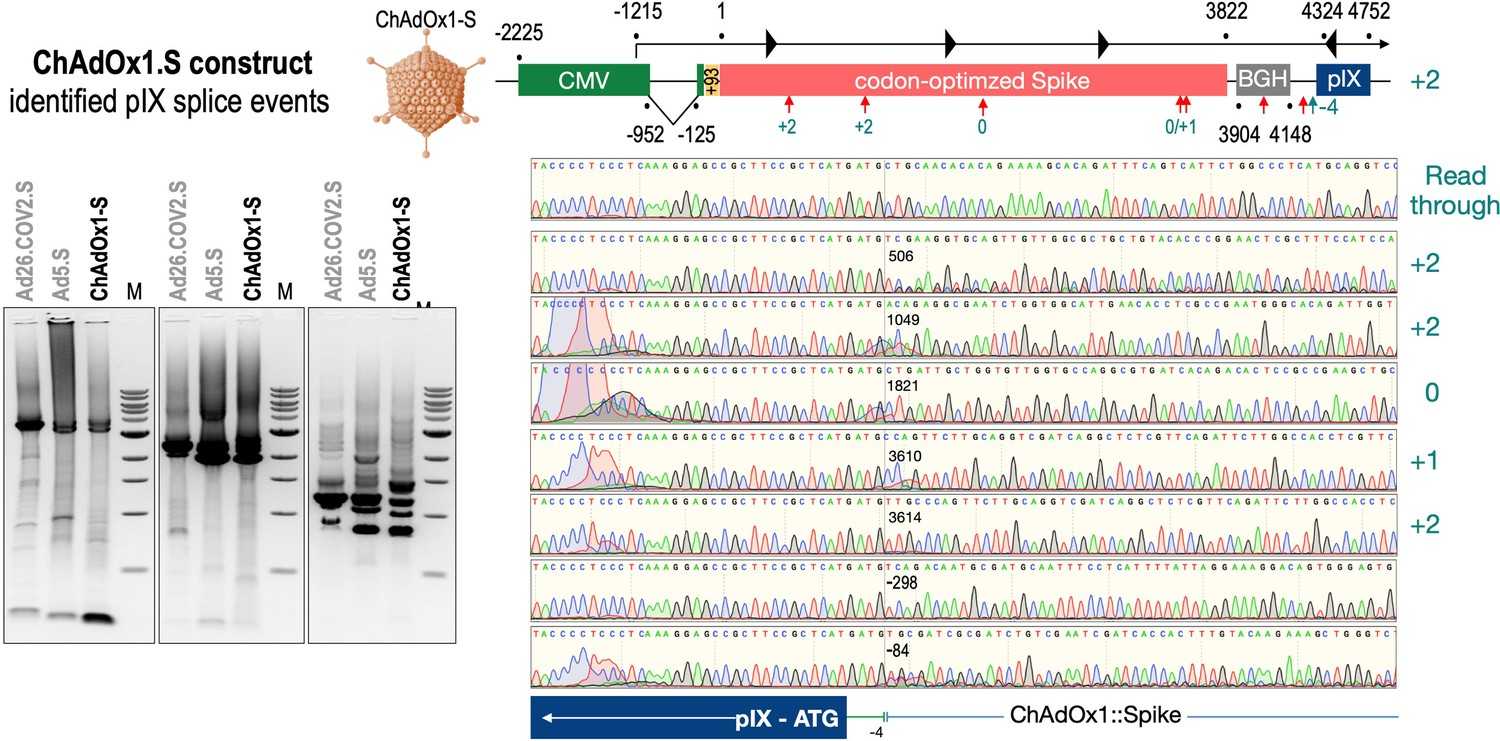
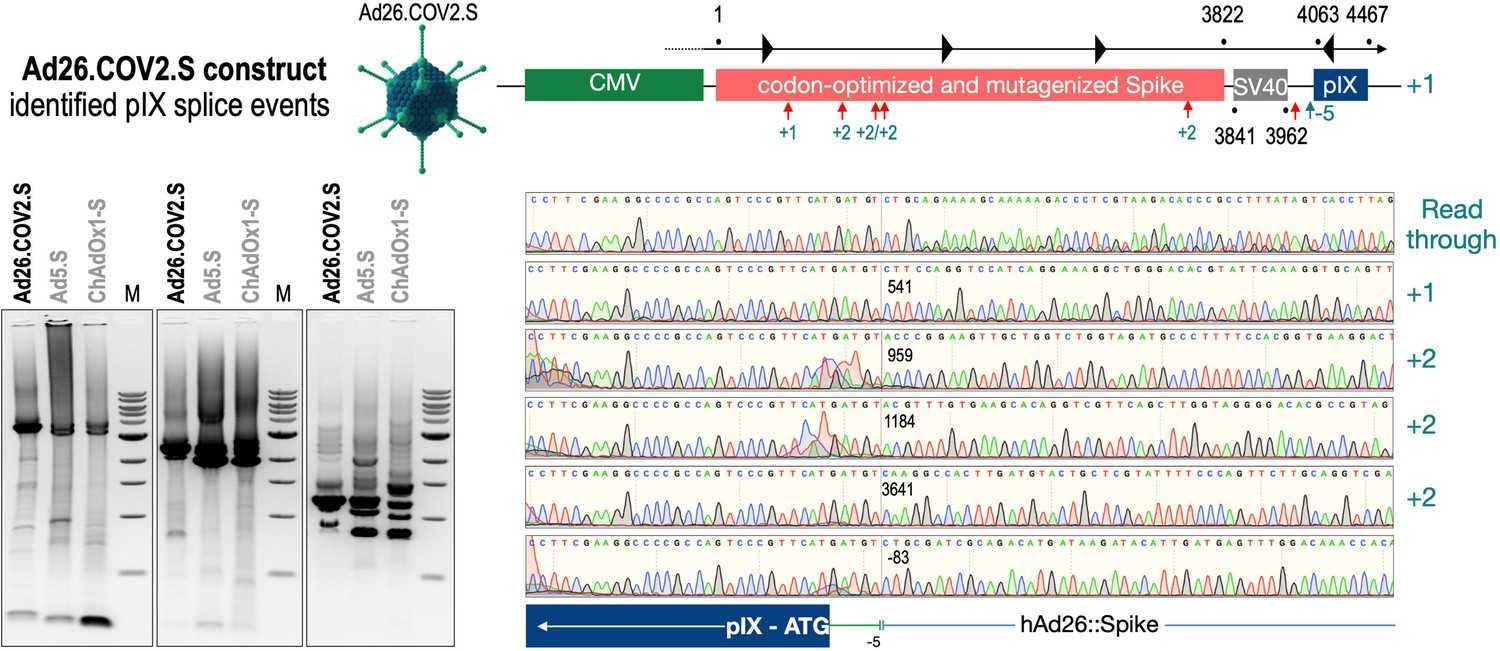
Биологи считают, что создателям вакцин нужно поместить спайк-белок на аденовирусном векторе в таком месте, чтобы свести к минимуму неправильный сплайсинг. Таким образом удастся избавиться от побочных эффектов векторных вакцин.
Автор: Анастасия Кузнецова-Фантони
