Прионы-передатчики нейродегенеративных заболеваний, и прионы, которые повреждают нейроны, — это разные молекулы, сообщается в Proceedings of the National Academy of Sciences.
Это выяснилось в ходе экспериментов, в которых к питательной среде культур нервных клеток добавляли либо экстракт очищенных прионов (переносчики инфекций), либо гомогенизированную ткань мозга животных, демонстрировавших симптомы прионных заболеваний, в том числе нейродегенерацию. В первом случае клетки в культурах оставались нетронутыми, во втором повреждались.
Прионы — это белковые инфекционные агенты, а от прочих протеинов они отличаются способностью принимать очень устойчивые конформации и «заражать» ими соседние молекулы такого же состава. В результате белки особой, патологической конформации образуют скопления и деформируют клетки, в которых находятся. Особенно часто это происходит в нервных клетках, и многие прионные болезни поражают мозг. Повреждения получаются очень сильными и необратимыми, и больной, как правило, погибает. Лечения прионных заболеваний пока не существует.
Прионные заболевания могут быть наследственными, если имеются мутации в генах соответствующих белков. Кроме того, ими можно заразиться, если съесть мозг или мясо инфицированных особей (термическая обработка и многие пищеварительные ферменты, как правило, не разрушают прионные скопления) или вступить в контакт с жидкостями их тела. Однако на молекулярном уровне детали заражения прионными инфекциями еще неясны.
Исследователи из Университетского колледжа в Лондоне во главе с Джоном Коллинджем (John Collinge) проверили, как действуют на первичные культуры нейронов (то есть «готовые» нервные клетки, изъятые непосредственно из организма животного) новой коры больших полушарий и гиппокампа мышей различные прионы.
К питательной среде, в которой находились одни культуры, исследователи на 72 часа добавляли в разных концентрациях очищенные палочковидные скопления молекул прионного белка, кодируемого геном Prnp, выделенные из мозга мышей с симптомами прионного нейродегенеративного заболевания (от 107,7 до 108,1 инфекционных единиц на миллилитр). В других случаях вместо очищенных белков использовали гомогенизированную ткань мозга больных мышей, в ней содержалось от 104,2 до 105,7 инфекционных единиц прионов на миллилитр. Наконец, в часть культур ввели гомогенаты мозга здоровых животных, куда предварительно добавили очищенные «заразные» прионные белки. Для контроля использовали белки со «здоровой» конформацией, не способные инфицировать клетки.
За состоянием нейронов в культуре — количеством, длиной и степенью ветвления их отростков, а также тем, живы ли они, наблюдали с помощью флуоресцентной микроскопии: подбирали к молекулам, характерным для разных регионов и функциональных состояний нервной клетки, антитела, связанные с флуоресцентными белками, дающими свечение разных цветов, и смотрели, где и с какой интенсивностью оно проявится.
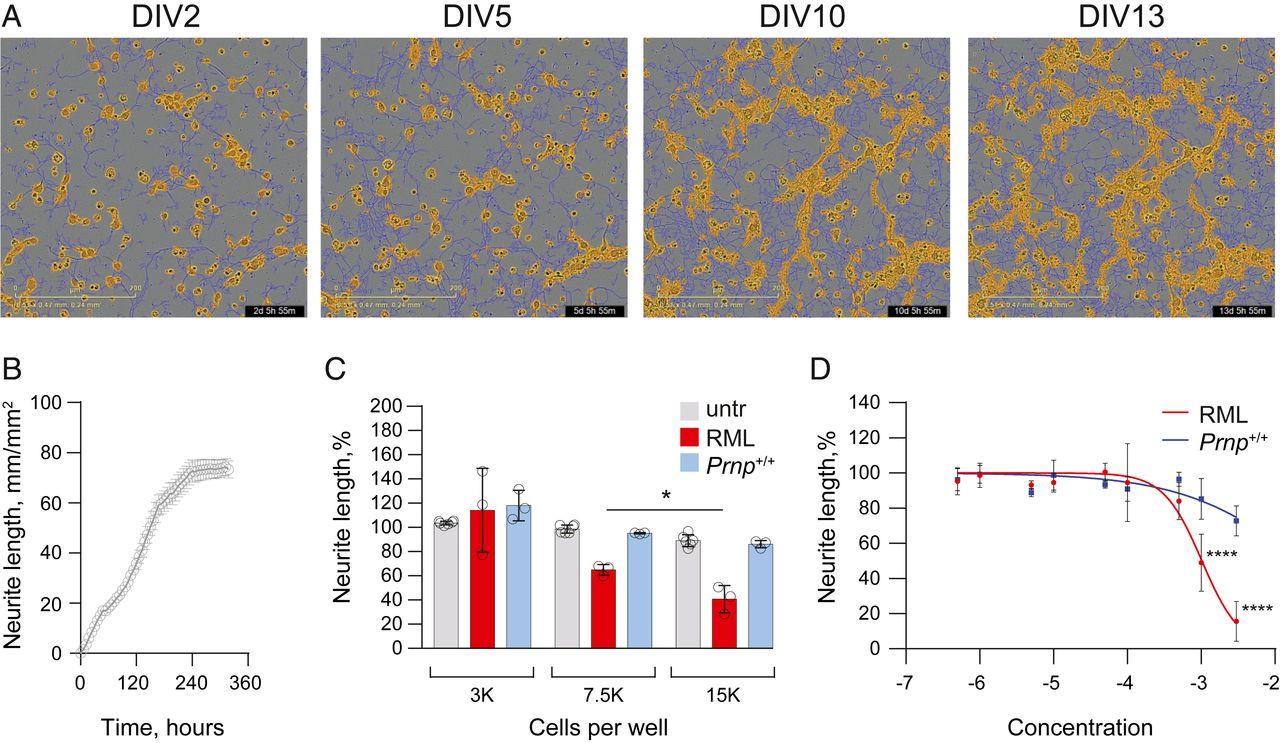
Длина отростков нервных клеток и количество выростов на них уменьшались только в одном случае — когда к культуральной среде добавляли гомогенат мозга мышей с прионным заболеванием. Очищенный прион из тканей больных животных, в том числе в составе гомогената мозга здоровых грызунов, не вредил нейронам, как и очищенный «безопасно сложенный» прионный белок из них. Нейротоксический эффект гомогенизированного мозга больных мышей исчезал под действием двухпроцентного натрий лауроилсаркозина — вещества, которым в ряде случаев обрабатывали гомогенаты. При этом количество молекул инфицирующего приона не снижалось.
Из этих данных исследователи сделали вывод, что у прионов функция заражения клеток и токсическое действие на эти клетки не связаны жестко друг с другом. Вероятно, они обеспечиваются различными типами молекул и (или) формами их скоплений. Видимо, прионы, образующие палочковидные скопления, нетоксичны для нейронов, а белки в составе скоплений какой-то другой формы, напротив, им вредят. Известно, что плохо очищенные прионы повреждают нервные клетки, но в предыдущих исследованиях не уточнялось, какой формы должны быть их группы, чтобы быть токсичными. Это и непросто установить: в таких смесях встречаются прионные скопления самых разных форм и размеров. Новые исследования должны быть направлены на то, чтобы все-таки это проверить.
Не вызывающие заболеваний прионы уже находили. В 2016 году итальянские ученые выделили из мозга овец, больных почесухой (скрейпи), молекулы PrPSc, размножили их, «адаптировали» под строение прионов у восприимчивых к скрейпи рыжих полевок (Myodes glareolus) и попробовали этими веществами инфицировать грызунов. Одна из разновидностей PrPSc овец по какой-то причине не могла спровоцировать у полевок почесуху — вероятно, из-за особенностей структуры молекулы.
Автор: Светлана Ястребова