В конце прошлой недели многие отечественные СМИ – от правительственной «Российской газеты» до респектабельного Esquire опубликовали сенсационную новость: «Ученые из Японии оживили на несколько недель мозг мыши» [1, 2].
Правда, нашлись критики исследования, действительно опубликованного в научном журнале Analytical Sciences — дескать, журнал слабоват (Impact Factor журнала на 2017/1018 годы действительно невелик, 1,618, хотя в России журналов с таким импактом – единицы). Однако неправы ни те, ни другие. Журнал просто специализированный, а ученые вообще ничего не воскрешали, и в статье об этом – ни слова.
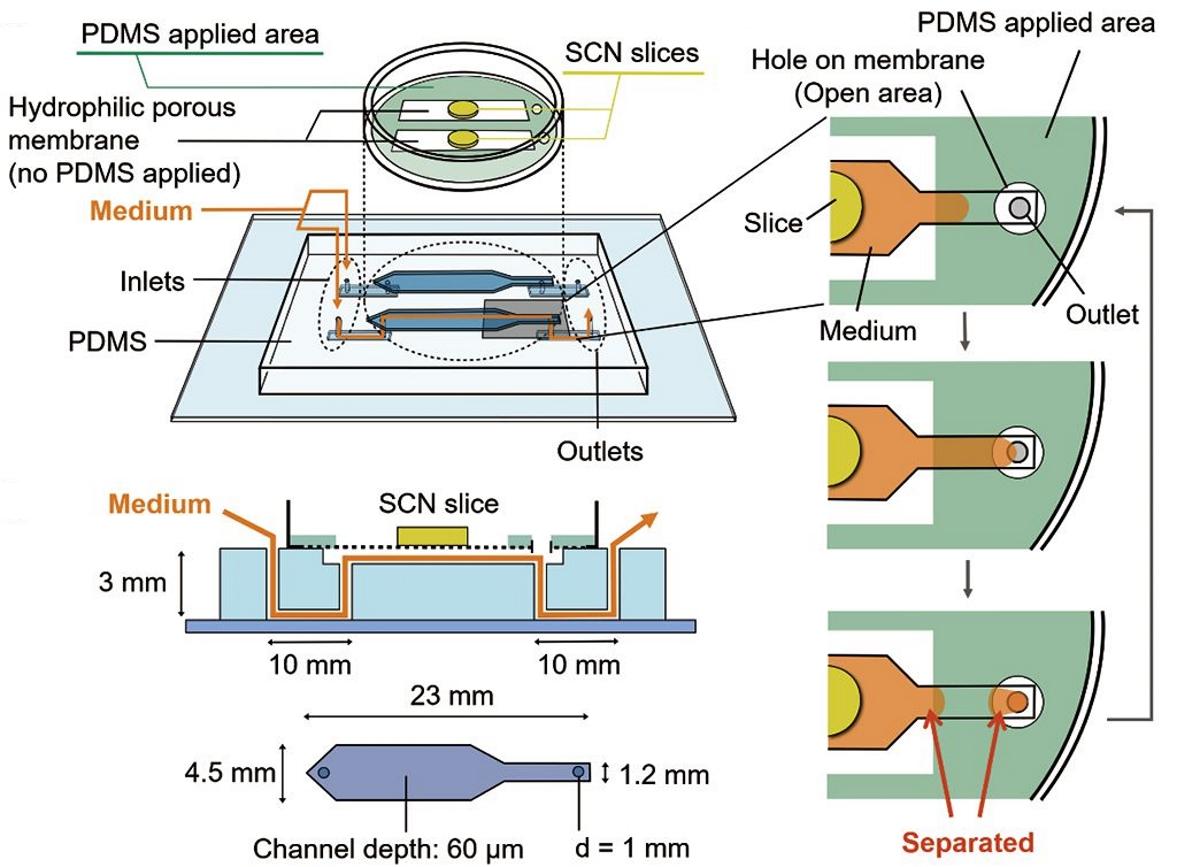
Действительно, издание – журнал японского Общества аналитической химии, и, кстати, 1,618 – это один из самых высоких импактов у японских химических журналов (годом раньше импакт журнала был равен 1,355). А название статьи, которая опубликована исследователями из одного из мощнейших институтов по исследованию мозга в мире, RIKEN, не имеет никакого отношения к оживлению. Вот как она называется: A Microfluidic Platform Based on Robust Gas and Liquid Exchange for Long-term Culturing of Explanted Tissues. То есть авторы в ней сообщают, что им удалось создать микрофлюидную платформу (на таких делают знаменитые «органы-на-чипе»), в которой высоконадежный газо-жидкостный обмен позволил долгое время культивировать экспланированные (то есть, удаленные из живого организма) ткани.
То есть речь вообще не идет ни об оживлении мозга, ни даже о сохранении удаленного из живого организма органа целиком. Что же сделали исследователи в эксперименте?
Микрофлюидные устройства, которые доставляют питательные вещества и газы в извлеченные из организма ткани мозга, используются уже давно. Однако они позволяют оставлять живыми их на временном отрезке от нескольких часов до нескольких дней. Однако для исследователей этого мало – иногда им нужно несколько недель. Особенно это касается изучения такого замечательного участка головного мозга, как супрахиазматического ядра (SCN), которое отвечает за циркадные ритмы. Этим-то и озаботилась группа авторов во главе с Нобутоси Ода из Центра исследований биосистемной динамики RIKEN.
Они предложили новую микрофлюидную систему на основе полидиметилсилоксана с пористой гидрофильной фторопластовой мембраной. Эта система, омывая ткани, должна была не разрушать их структуру, как это часто происходит – и решили проверить, как она будет работать на эксплантированном супрахиазматическом ядре мыши. Но не обычной, а так называемой нок-ин-мыши, в которой ген PER2, который кодирует один из главных белков циркадных ритмов, period2, экспрессировался совместно с встроенным в геном геном (в этих словах – разные ударения) люциферазы. Таким образом, когда ген PER2 экспрессировался, одновременно синтезировался и светящийся белок, который хорошо виден и показывает, что ткань еще жива.
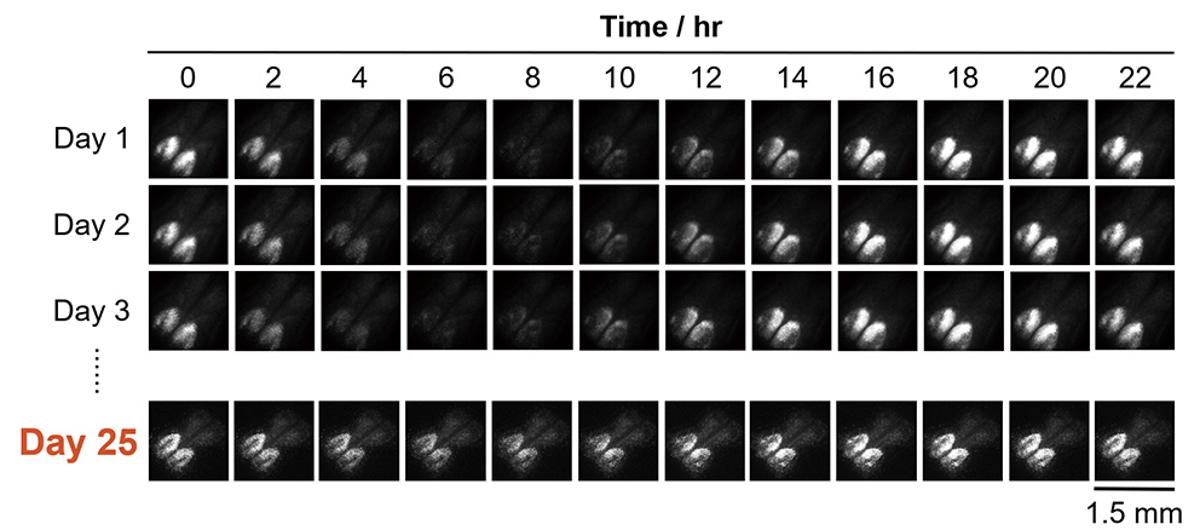
Да, к слову о ткани: в микрофлюидное устройство помещали даже не все супрахиазматическое ядро целиком, а его срезы (получается, как в анекдоте – не мозг, а небольшую его часть, и не часть – а ее срезы).
Что же вышло? Действительно, срезы SCN в разработанном устройстве светились на протяжении как минимум 25 дней после начала эксперимента, показывая периодическую экспрессию гена PER2, срезы в «обычной» установке потухли на пятый день. Говорят, устройство должно работать до сотни дней, и авторы подозревают, что их система может стать стандартной платформой для поддержания жизнеспособности срезов мозга для научных исследований.
Сухой остаток: никакого оживления мозга не было, хорошими исследователями из хорошего научного учреждения создана прекрасная платформа, которая потенциально может помочь в изучении работы живого мозга. А «ученый снова изнасиловал журналиста» (с).
Текст: Алексей Паевский
