Ученые из США выяснили, что за тягу к соли у животных и человека отвечают узкоспециализированные нейроны в головном мозге, которые активируются гормоном альдостероном.
Вводя мышам гормон непосредственно в мозг и подкожно, исследователи обнаружили, что альдостерон в высоких дозах способен проникать через гематоэнцефалический барьер и активировать группу из нескольких сотен нейронов, заставляя их обладателя отправляться на поиски соли, в то время как удаление этих нейронов блокирует тягу к соли. Результаты опубликованы в журнале JCI Insight.
Чрезмерное потребление соли вредно, но полный отказ от соли может привести к смерти. Соль содержит натрий, который отвечает за кислотно-щелочной и водный баланс организма, а также участвует в создании мембранного потенциала и проведении возбуждения в нервных и мышечных клетках. Натрий поступает в организм из пищи и выделяется почками; за процессы реабсорбции катионов натрия отвечает минералокортикоидный гормон альдостерон, вырабатываемый в коре надпочечников.
Дефицит натрия в организме вызывает острое желание съесть что-нибудь соленое, таким образом активируется поисковое поведение, цель которого — найти соль. Более 15 лет назад Джоэл Герлинг (Joel C. Geerling) открыл нейроны, главная функция которых заключается в запуске такого поведения. Они находятся в продолговатом мозге в ядре одиночного пути и экспрессируют рецептор, способный связываться с альдостероном, а также фермент 11-бета-гидроксистероиддегидрогеназу 2 (HSD2), регулирующий работу этого рецептора.
В своей новой работе Джоэл Герлинг с группой ученых из Университета Айовы продемонстрировал, что аналогичные нейроны HSD2 есть также у человека и у свиней, и находятся они в тех же самых областях мозга, что у крыс и мышей. К таким выводам ученые пришли после анализа тканей из ствола мозга 12 человек (в возрасте от 33 недель до 77 лет), скончавшихся от разных неврологических патологий. Человеческие нейроны HSD2 имеют веретенообразную форму с двумя — тремя первичными дендритами. В стволе мозга человека, по оценкам исследователей, содержится 958 плюс — минус 320 таких нейронов (это всего лишь 0,000001 процент из 86 миллиардов нейронов в человеческом мозге), что примерно в два раза больше, чем у крыс, и в четыре-пять раз больше, чем у мышей. Сходство нейронов HSD2 у грызунов, свиней и человека позволяет предположить, что они являются эволюционно консервативным компонентом мозга млекопитающих.
В ходе экспериментов дефицит натрия в пище мышей повышал выработку альдостерона, активировал нейроны HSD2 и, как следствие, вызывал жажду натрия, — они увеличивали потребление физраствора (трехпроцентный раствор NaCl) при прежнем потреблении воды. Недели потребления пищи с дефицитом натрия оказалось достаточно, чтобы активировать «солевые» нейроны.
Для определения значимых концентраций альдостерона ученые вводили гормон непосредственно в IV желудочек головного мозга мышам, которые были распределены на восемь групп: контрольную, получавшую только воду (четверо животных) и семь групп, получавших альдостерон в разных концентрациях: 1 (трое животных), 2,5 (двое животных), 5 (шесть животных), 10 (пять животных), 25 (пять животных), 50 (четверо животных) и 100 нанограмм в час (пять животных). Для оценки влияния периферического альдостерона ученые отобрали несколько групп мышей, которым гормон вводился подкожно: контрольная группа (четверо животных) и шесть групп, получавших альдостерон в концентрациях, существенно более высоких, чем получали мыши, которым гормон вводили в мозг — 10 (двое животных), 100 (трое животных), 250 (трое животных), 500 (пять животных), 750 (трое животных) и 1000 нанограмм в час (шесть животных).
Ученые сообщают, что чем больше гормона вводили мышам до определенного предела, тем больше физраствора животные выпивали, то есть, эффект был дозозависимым. Количество альдостерона, необходимое для активации поискового поведения, зависело от того, куда именно вводили гормон: если прямо в мозг, то альдостерона требовалось немного, если же гормон вводили подкожно, то его нужно было в 100 раз больше для аналогичной активации нейронов HSD2 в мозге (10 нанограмм в час при внутримозговом введении и 1000 нанограмм в час при подкожном). Это объясняется тем, что альдостерон с трудом проходит через гематоэнцефалический барьер, и для того, чтобы запустить поведение, связанное с поиском соли или других натрийсодержащих продуктов, требуется выраженный длительный дефицит натрия. Удаление нейронов HSD2 снижало тягу мышей к соли: спровоцированный альдостероном аппетит к натрию полностью пропадал после удаления 50 процентов нейронов HSD2.
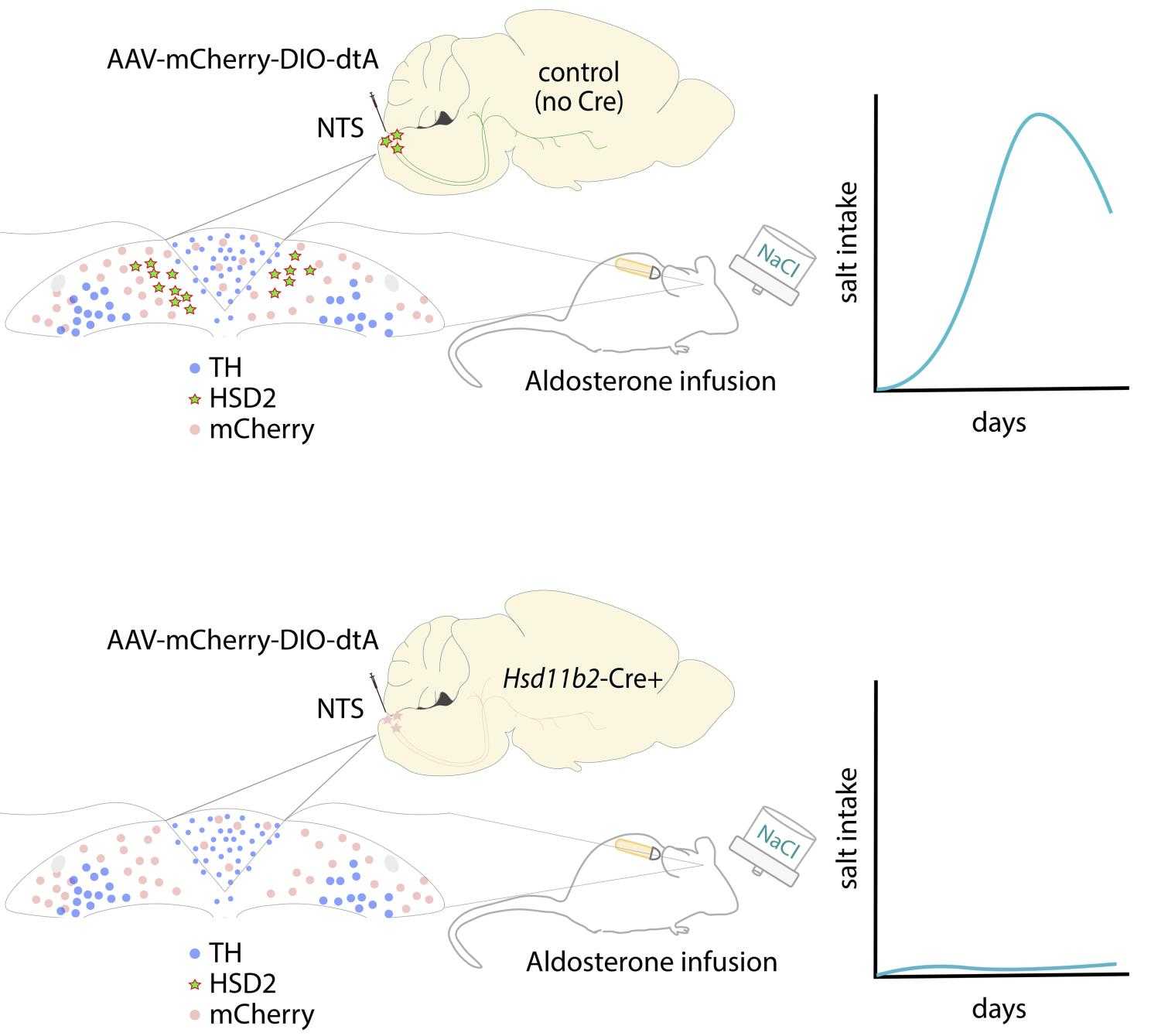
По словам ученых, ранее было непонятно, зачем при хроническом дефиците натрия организм тратит массу энергии на гипертрофию надпочечников, позволяющую значительно увеличить концентрацию циркулирующего в крови альдостерона (до 10-20 наномоль) — это намного больше, чем требуется для активации рецепторов в периферических клетках организма, экспрессирующих HSD2. Теперь же исследователи считают, что таким образом альдостерон может проникнуть через гематоэнцефалический барьер и попасть в мозг, чтобы активировать животное на поиск натрия.
Большинство здоровых людей потребляет достаточно натрия, и скорее всего их организм никогда не будет вырабатывать альдостерон в дозах, необходимых для преодоления гематоэнцефалического барьера. Повышенные показатели альдостерона (более 300 миллиграмм на децилитр) могут быть достигнуты в результате диеты с повышенным содержанием калия и дефицитом натрия. Высокие концентрации циркулирующего альдостерона обнаружены также у пациентов с аденомами, секретирующими альдостерон, и с хроническими заболеваниями почек. Дальнейшие исследования высокоспецифичных нейронов HSD2 могут помочь найти терапевтическую мишень для заболеваний, связанных с нарушением выработки альдостерона.
Автор: Юлия Нестерова