Если клетки микроглии, так называемый «иммунитет» ЦНС, мутируют, то у человека во взрослом возрасте развивается лейкоэнцефалопатия, лечения для которой на данный момент не существует.
При этом заболевании постепенно начинает разрушаться белое вещество мозга, ухудшая работу и двигательных, и когнитивных центров. Ученые продемонстрировали, что пересадка здорового красного костного мозга и подавление работы мутировавшего гена восстанавливает потерянные функции у мышей и останавливает развитие заболевания у людей. Исследование опубликовано в журнале Science.
Микроглия – важный тип иммунных клеток центральной нервной системы. Эти клетки окружают и защищают нейроны от патогенов и при повреждениях, способствуют нейропластичности, задействованы при нейродегенеративных заболеваниях вроде болезни Паркинсона, а частичная дисфункция микроглии приводит к развитию нервно-психических расстройств вроде депрессии.
Ген, кодирующий рецептор колониестимулирующего фактора 1 или CSF1R, считается одним из ключевых генов микроглии, обеспечивающих нормальное функционирование и жизнедеятельность клеток. Мутация в этом гене у микроглиальных клеток имеет два исхода: в случае, если мутация произошла в обоих аллелях (вариантах гена), то еще на пренатальном уровне развития она ведет к летальному исходу; в случае же мутации только в одном аллеле наблюдается CSF1R-ассоциированная микроглиопатия (CAMP). Иными словами, случай, когда из-за мутации в гене CSF1R нарушается адекватная работа микроглии.
Именно нейроглиопатия становится наиболее распространенной формой лейкоэнцефалопатии взрослых с аксональными сфероидами и пигментированной глией (ALSP). Этот сложный диагноз подразумевает то, что из-за дисфункции микроглии у пациента во взрослом возрасте начинается отмирание белого вещества головного мозга, спад когнитивных и двигательных функций. Болезнь всегда приводит к летальному исходу, а терапии на данный момент не существует.
Одним из потенциальных методов лечения этого тяжелого неврологического заболевания ученые считают пересадку пациенту здоровой микроглии и подавление генетически измененной. Поскольку микроглия относится к иммунным клеткам, ее формирование и развитие происходит в красном костном мозге. По этой причине ученые вместо значительно инвазивной пересадки здоровой микроглии пациенту предпочли исследовать пересадку здорового костного мозга как один из вариантов лечения.
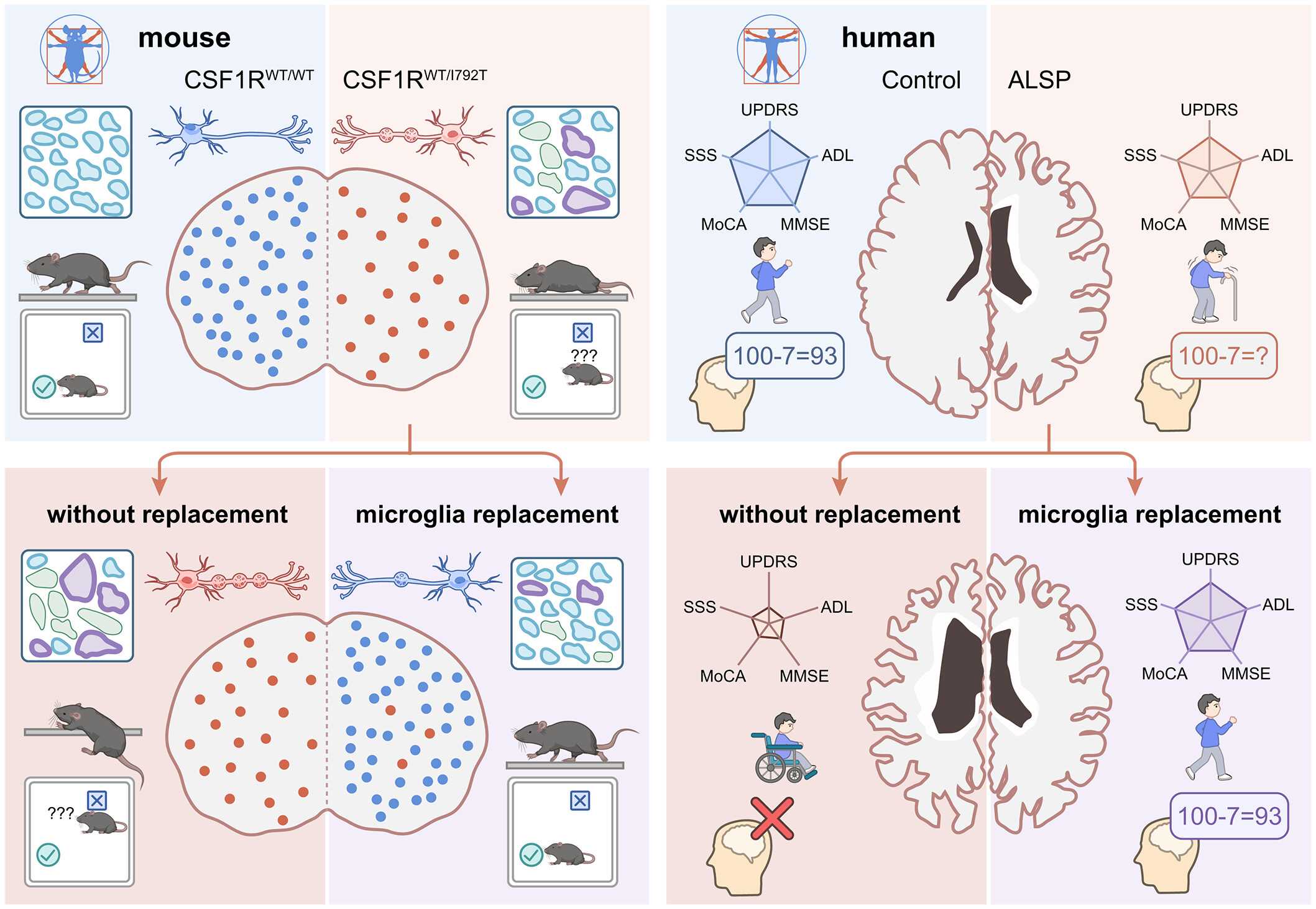
Чтобы протестировать эффективность такого подхода, ученые создали модели мышей с генетическими мутациями, в точности повторяющими характерные черты CAMP, среди которых были уменьшение количества глиальных клеток, патологии миелина, набухание аксонов нейронов, нарушение двигательной активности и когнитивных способностей. Этим мышам с ALSP ученые пересадили красный костный мозг здоровых мышей и заблокировали работу мутантного аллеля CSF1R в уже имеющихся клетках микроглии.
В результате этих действий в течение нескольких месяцев у мышей практически остановилось развитие заболевания, улучшились сенсорное восприятие, движения и когнитивные функции. Помимо этого изменились и клетки, окружающие микроглию: одноклеточное секвенирование РНК разных типов клеток показало, что после лечения олигодендроциты (другой тип глиальных клеток, формирующих миелин) вернулись к более адекватному фенотипу, а сигнальные пути между клетками микроглии стали здоровее.
Достигнув таких результатов на мышиных моделях, ученые решили провести первые клинические испытания на людях. Для этого было отобрано 8 добровольцев с ALSP, которым провели пересадку здорового костного мозга. За пациентами велось активное наблюдение в течение двух лет. С помощью неинвазивного ПЭТ сканирования мозга ученые обнаружили, что со временем углеводный обмен в мозге вырос, что косвенно свидетельствует о восстановлении функций микроглии. Помимо этого, МРТ сканирование мозга и клинические оценки состояния пациентов показали, что разрушение белого вещества в мозге практически остановилось, а когнитивные и двигательные функции не ухудшались в течение всего периода наблюдения.
«Важное клиническое значение имеет тот факт, что пересадка красного костного мозга остановила прогрессирование заболевания у четырех человек, что позволяет предположить, что это может быть эффективной терапевтической стратегией для лечения CSF1R-ассоциированных заболеваний», – прокомментировала результаты исследования редактор журнала Nature Маттиа Марозо.
В будущем ученые планируют совершенствовать эту технологию и адаптировать ее под восстановление функций микроглии.
Текст: Рената Тулакина