Нейроинтерфейс, соединяющий спинной и головной мозг, позволил пациенту с повреждением спинного мозга лучше ходить — сначала со стимуляцией, а потом и без нее.
Для создания такого цифрового моста исследователи и врачи из Швейцарии с коллегами из Великобритании, США и Франции объединили электростимуляцию спинного мозга и расшифровку сигналов головного мозга. О результатах они рассказали в журнале Nature.
Чтобы мы могли ходить, нейроны в пояснично-крестцовом отделе спинного мозга должны обмениваться сигналами с нейронами головного мозга. Повреждение спинного мозга выше этого отдела может нарушить эту связь — тогда команды из головного мозга до мышц ног доходить не будут, и возникнет паралич.
Уже несколько лет ученые с помощью эпидуральной электростимуляции спинного мозга пытаются ставить парализованных на ноги. Команда швейцарских исследователей начинала с крыс, продолжила макаками, а после успешных экспериментов перешла на людей. Принцип такой: электроды помещают между позвоночником и спинным мозгом и с их помощью стимулируют нужные нервные окончания — то есть имитируют сигналы, которые должны поступать из головного мозга. Такая стимуляция позволяла прежде парализованным людям стоять, двигать ногами, ходить, ездить на велосипеде и заниматься греблей.
Однако обычно пациентам с имплантированными в позвоночник электродами приходится носить еще и датчики движения. Эти датчики отслеживают движения мышц и помогают выбирать сигнал, который следует послать в спинной мозг дальше. Это не слишком похоже на естественный контроль движения, а ходить пациенты могут (если вообще могут) только с опорой и только по беговой дорожке или ровным поверхностям.
Теперь нейрохирург Грегуар Куртин (Grégoire Courtine) из Федеральной политехнической школы Лозанны и его коллеги создали цифровой мост, соединяющий головной мозг со спинным, и таким образом заместили нервные пути, которые были повреждены. Устройство испытали на мужчине 38 лет, который десять лет назад упал с велосипеда и получил неполную травму спинного мозга и перестал ходить.
Несколько лет назад пациент уже участвовал в клиническом испытании: это была пятимесячная программа нейрореабилитации, основанная на все той же эпидуральной стимуляции спинного мозга. Тогда стимуляция помогла ему снова начать ходить — с помощью ходунков с колесом. Также удалось восстановить частичную подвижность без стимуляции. Еще три года мужчина применял стимуляцию дома, но ходить он мог только по плоским поверхностям, и ему было трудно останавливаться и снова начинать движение. Подниматься и спускаться по пандусам или лестницам он не мог. Тогда он решил поучаствовать в новом исследовании.
Сначала ученые выяснили, какие именно области коры мозга пациента больше всего вовлечены в попытки двигать ногами — это нужно было, чтобы понять, где размещать имплантаты, которые будут считывать сигналы.
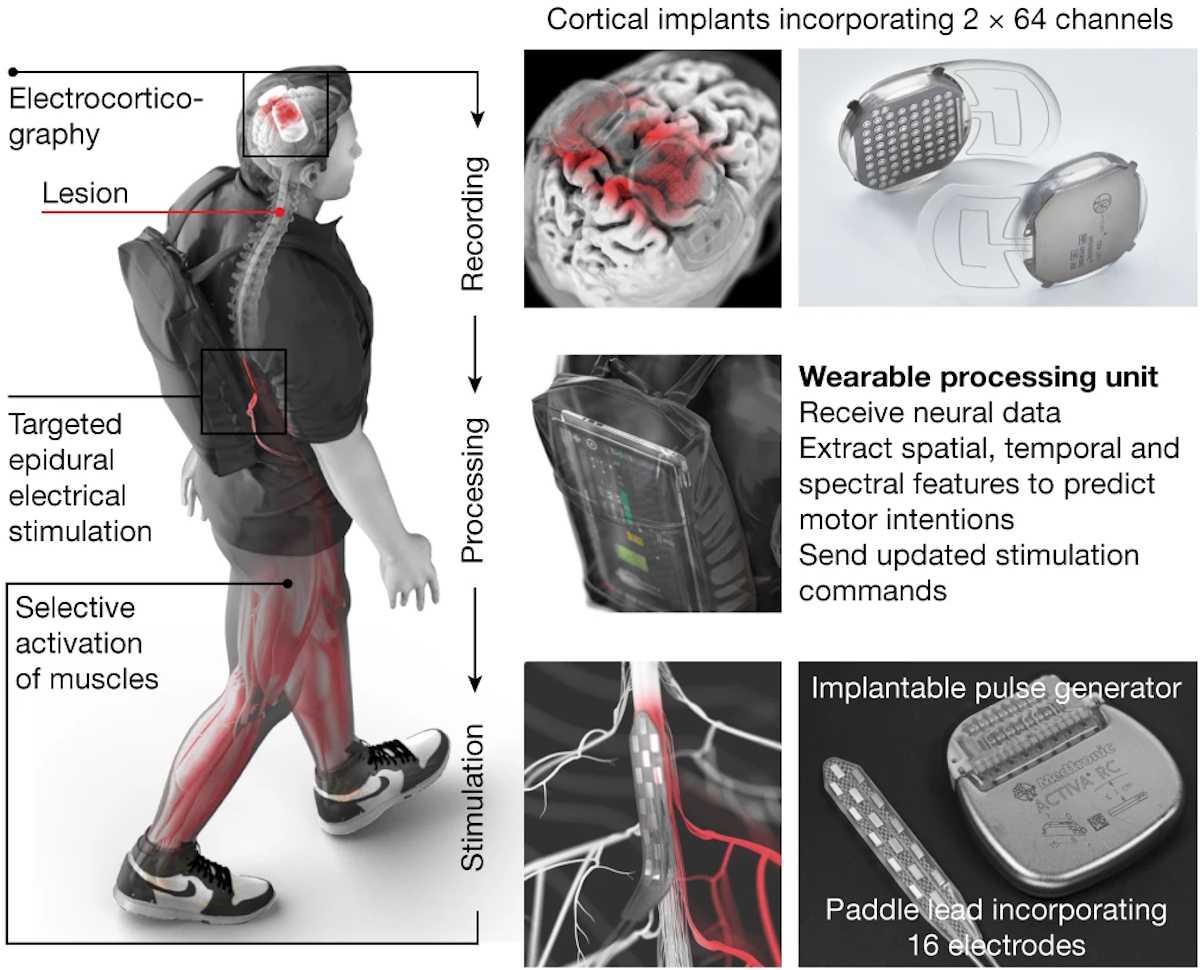
Имплантаты — это 2 титановых круглых корпуса диаметром 5 сантиметров, внутри которых сетка из 64 электродов. Врачи встроили их в череп пациента, присоединив электроды к твердой мозговой оболочке левого и правого полушария.
Записанные сигналы мозга ловила антенна на внешней гарнитуре (ее пациент носил в рюкзаке за спиной) и передавала их в режиме реального времени на процессор — тот на основе этих сигналов прогнозировал двигательные намерения. Затем эти двигательные намерения преобразовывались в новые сигналы, которые обрабатывал тот же процессор.
Дальше команды поступали на генератор импульсов ACTIVA RC, который имплантировали под кожу на животе пациента. Генератор передавал электрические импульсы на корешки спинного мозга с помощью матрицы из 16 электродов на имплантированном лопастном проводе Specify 5-6-5. Эти электроды остались в спинном мозгу пациента еще со времен прошлого исследования.
После завершения всех операций исследователи настроили устройство: сначала они просили пациента попытаться посгибать ноги в тазобедренном суставе, в коленях и в голеностопе, и отслеживали сигналы с моторной коры. Так они выяснили, какие именно электроды считывают каждый двигательный импульс. Затем они настраивали частоту и амплитуду стимуляции спинного мозга так, чтобы нужные сигналы приводили к сокращению и расслаблению нужных групп мышц.
Объединял все это алгоритм: одна модель вычисляла вероятность намерения согнуть или разогнуть конкретный сустав, а вторая предсказывала амплитуду и направление предполагаемого движения. С помощью этого алгоритма контроллер регулировал амплитуду стимулов, которые направлялись в спинной мозг.
Мужчина прошел 40 сеансов нейрореабилитации — у него улучшилось сгибание ног и он смог ходить с костылями с работающим устройством. Он останавливался, стоял, снова начинал идти. Двигать ногами и стоять самостоятельно он мог и раньше, но анализ показал, что держать баланс с устройством ему было даже легче. И, по его собственным ощущениям, мост позволял ему контролировать движения лучше, чем простая эпидуральная стимуляция. Кроме того, система позволила мужчине ходить по лестницам и неровной поверхности — то, чего раньше он не мог.
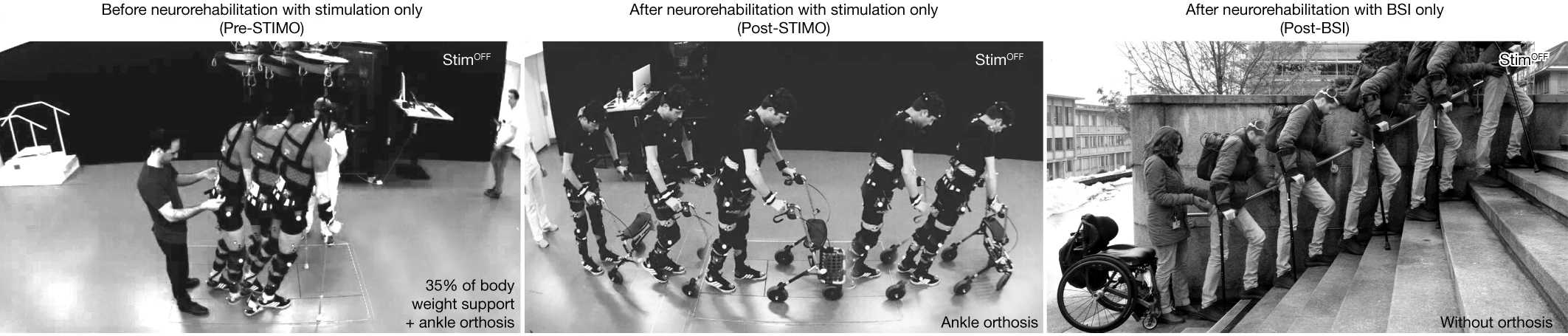
Интерфейс работал очень стабильно, и в конце концов пациент смог начать ходить со стимуляцией даже дома, без присмотра врачей. Даже спустя год сигналы не стали менее точными. Впоследствии пациент смог самостоятельно с костылями ходить по дому, стоять, садиться в машину и выходить из нее даже без стимуляции.
Авторы отмечают, что неизвестно, смогут ли пациенты с другими травмами спинного мозга использовать устройство, — поскольку проверяли его на конкретном и частичном повреждении. Но эпидуральная стимуляция уже помогала другим пациентам — в том числе с полным сенсорномоторным параличом, декодирование сигналов мозга тоже не ново, а откалибровать устройство достаточно просто. Поэтому каких-то серьезных помех для применения нейроинтерфейса у других пациентов ученые не видят.
Электростимуляция спинного мозга может помочь двигать не только ногами, но и руками — ученые из США вернули таким образом подвижность рук людям после инсульта. Но в этом случае электроды имплантировали в шейный отдел.
Автор: Катерина Петрова