Пигментный ретинит — наследственное заболевание, при котором сильно ухудшается зрение и часто наступает слепота. Испанские исследователи приблизились к тому, чтобы раскрыть ключевые механизмы этой генетической патологии глаз, что позволит в будущем разработать лечение.

Сетчатка — внутренняя оболочка глаза — особенно уязвима к генетическим и экологическим изменениям, которые вызывают окислительный стресс и повреждают клетки фоторецепторов и нейронов сетчатки, в итоге приводя к их гибели. Ученым известно примерно 90 генов, связанных с пигментным ретинитом, один из которых — CERKL (CERamide Kinase-Like). Мутации в этом гене вызывают пигментный ретинит и палочко-колбочковую дистрофию. Оба заболевания характеризуются дегенерацией фоторецепторов и прогрессирующей потерей зрения. Ген CERKL отвечает за устойчивость к окислительному стрессу. Его сверхэкспрессия защищает клетки от гибели из-за окислительного стресса. Также CERKL участвует в формировании стрессовых гранул и регулирует динамику митохондрий в сетчатке.
Сетчатка постоянно подвергается световому, а значит, и окислительному стрессу. Чтобы с ним справиться, ее клетки должны активировать антиоксидантные механизмы. Подробнее разобраться, как в этом задействован ген CERKL, взялась группа ученых под руководством профессора Джеммы Марфани (Gemma Marfany) из Института биомедицины Барселонского университета. Их работу опубликовал журнал Redox Biology.
Для исследования ученые использовали взрослых трансгенных мышей-альбиносов, у которых ген CERKL удалили с помощью метода генной инженерии CRISPR-Сas9. Опыты на них с применением электрофизиологических методов впервые показали, что при отсутствии гена CERKL клетки сетчатки непрерывно испытывают стресс и прогрессивно дегенерируют, как это происходит у людей с пигментным ретинитом.
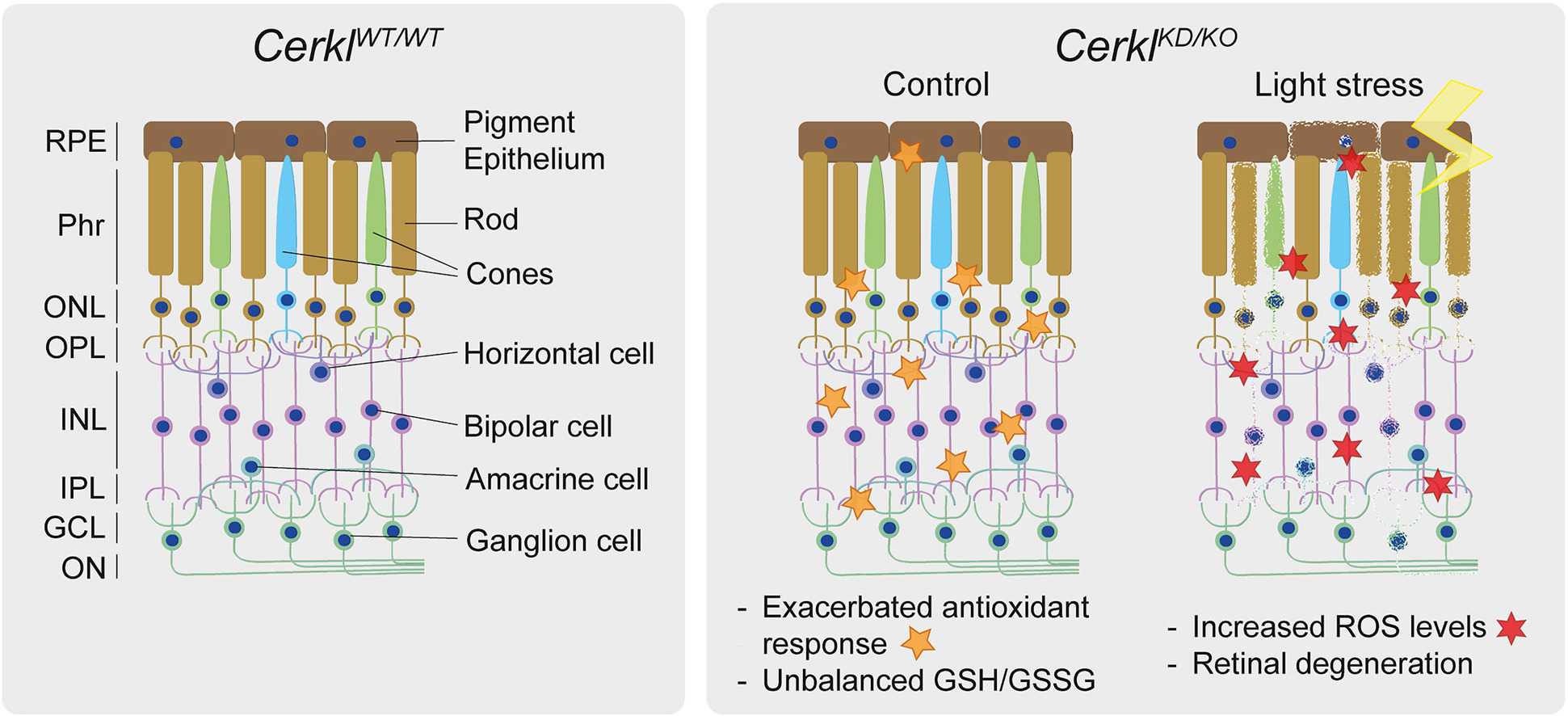
Во время экспериментов мышей обезболивали смесью кетамина и ксилазина, а затем на один глаз, предварительно закапанный циклопентолатом для расширения зрачка, в течение часа воздействовали белым светом яркостью 3000 люкс. Второй глаз при этом закрывали, чтобы использовать в качестве контрольной точки. По завершении процедуры мышей немедленно умерщвляли, а в полученной сетчатке ученые исследовали раннюю реакцию на световой стресс. В другой серии опытов, в которой изучали позднюю реакцию на стресс, световому воздействию подвергали сразу оба глаза, а умерщвление грызунов для получения тканей сетчатки происходило спустя две недели.
«При дополнительном окислительном повреждении — как в случае с продолжительной световой стимуляцией — клетки уже не в состоянии реагировать, поскольку не могут активировать механизмы антиоксидантного ответа. По этой причине сетчатка постоянно воспалена. Как следствие, в клетках сетчатки активируются механизмы клеточной гибели — некроптоз и ферроптоз», — рассказала Джемма Марфани.
Она добавила, что хотя эксперименты проводили на мышах, выявленные в сетчатке изменения позволяют объяснить, как и почему фоторецепторные клетки погибают у пациентов с пигментным ретинитом, вызывая слепоту.
Ученые назвали свои результаты важными, поскольку они дополняют имеющиеся генетические исследования и открывают путь к разработке новых подходов в терапии наследственных заболеваний глаз. Пигментный ретинит — наиболее распространенная форма наследственной дистрофии сетчатки. В целом болезни этой группы в мире встречаются у одного человека из трех тысяч.
Автор: Юлия Трепалина