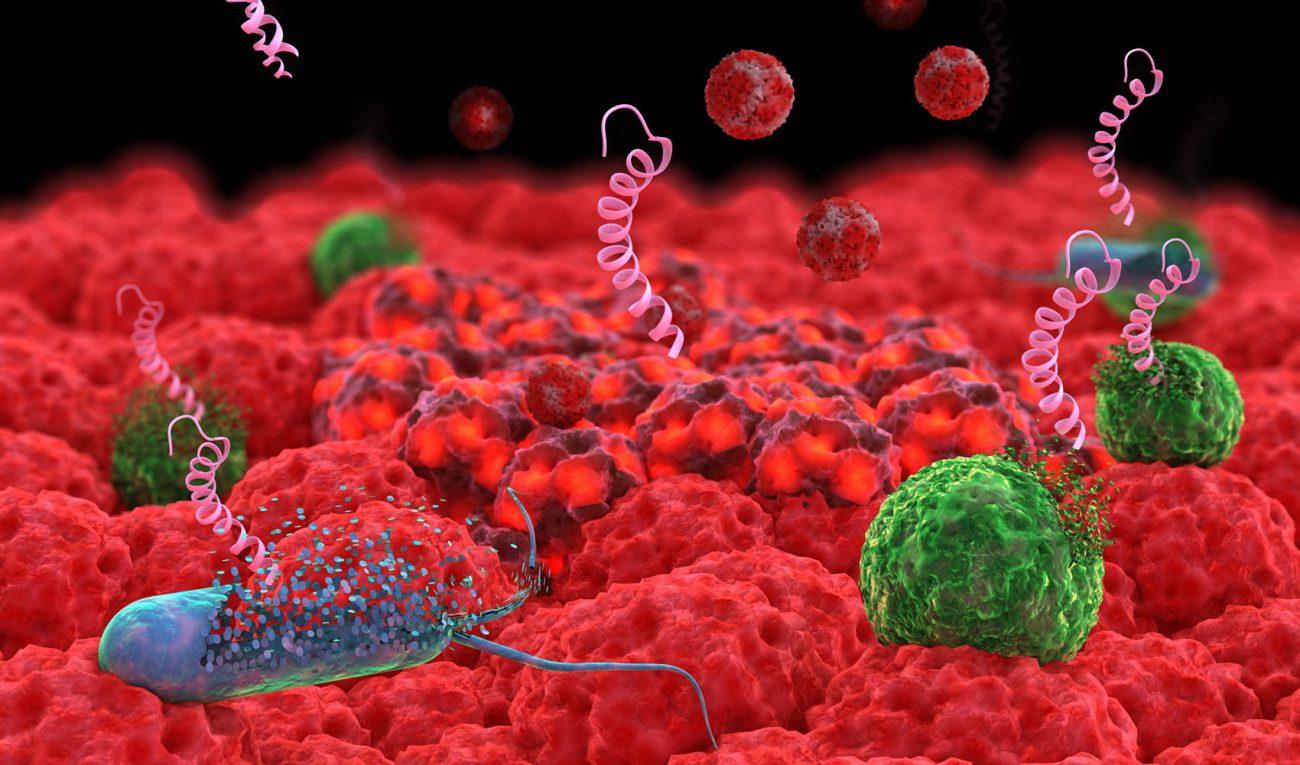
Лекарства, которые защищали нас от вездесущих бактерий больше семидесяти лет, медленно теряют свою хватку, и нам необходимо новое оружие в борьбе с инфекциями.
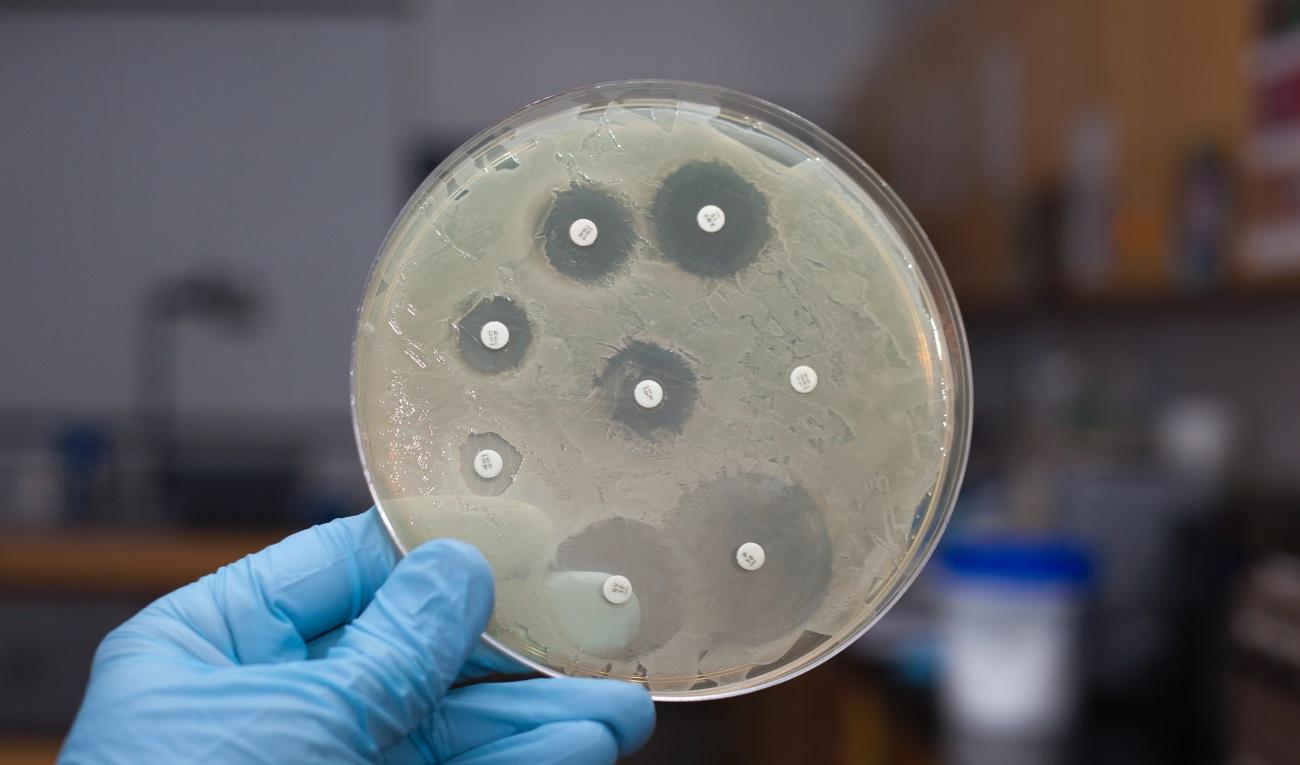
Болезнетворные бактерии становятся невосприимчивыми к антибиотикам, которые когда-то их истребляли, даже к таким лекарствам, которые некогда считались последней линией обороны.
Устойчивые к антибиотикам (антибиотикорезистентные) бактерии убивают примерно один процент людей, которых заражают, даже в развитых странах. И если это оставить без внимания, они будут убивать в пять раз больше людей ежегодно.
«Многие вещи, которые мы считаем сами собой разумеющимися в данный момент, вроде кесарева сечения, или замены тазобедренного сустава, или пересадки органов, без антибиотиков станут очень сложными», говорит Франсуа Франчески, руководитель программ терапевтического развития отделения бактериологии и микологии Национального института аллергии и инфекционных заболеваний.
Особенно уязвимы люди с ослабленной иммунной системой, но в постантибиотическом мире под угрозой будут все без исключения.
«Люди говорят, что в эпоху после антибиотиков антибиотики уже не смогут нам помочь даже с мельчайшей царапиной», говорит Сезар де ла Фуэнте, биоинженер из Массачусетского технологического института.
Для борьбы с резистентными бактериями мы обращаемся к новым союзникам, вроде вирусов, которые атакуют только бактерий; наночастиц и крошечных белков на основе вырабатываемых иммунными системами различных организмов. Каждый инструмент обладает своими преимуществами и недостатками, поэтому ученые изучают самые разные подходы.
«Многие люди в этой области в настоящее время ищут альтернативные стратегии, которые можно было бы добавить в наш арсенал», говорит Тимоти Лу, тоже из MIT. «Не то чтобы каждый из них пытался изобрести собственную серебряную пулю, которая будет спасать нас от бактерий до конца жизни, а скорее изучает проблему с разных сторон».
Вот несколько способов, которые могли бы помочь нам справляться с нежеланными бактериями.
Обезоружить захватчиков
Бактерий не всегда нужно убивать, чтобы нейтрализовать. Некоторые виды лечения атакуют микробов косвенно, лишая их оружия. Бактерии будут на месте, но последствия заражения не будут серьезными, а иммунная система получит шанс сразиться с инфекцией самостоятельно.
Если ваш препарат на самом деле не убивает бактерий, у них будет меньше стимулов вырабатывать сопротивление к нему. Появление устойчивости займет больше времени, поскольку бактерии не будут активно бороться с препаратом, говорит Франчески.
Многие бактерии выделяют токсины, которые повреждают клетки хозяина. Один из распространенных типов токсинов называется порообразующим — он пробивает отверстия в клетках. Его выделяют метициллинрезистентный золотистый стафилококк, кишечная палочка, листерии, бактерии сибирской язвы и яд змей, скорпионов и морских анемонов.
Лянфанг Чжан придумал, как свести эти токсины на нет. «Вы отнимаете оружие, и они становятся намного слабее», говорит Чжан, наноинженер Калифорнийского университета в Сан-Диего. Он покрывает наночастицы сладкой мишенью — мембранами, составленными из красных кровяных телец. Красная кровяная клетка выступает в качестве приманки, засасывая токсин, который в противном случае атакует здоровые клетки. «Она будто губка высасывает токсины», объясняет Чжан.
В своем первом исследовании он показал, что наногубки всасывают токсины без вреда для мышей. В этом году работа Чжана с наночастицами в качестве приманок стала одним из 24 проектов, получивших финансирование от Национальных институтов здравоохранения. Он надеется начать клинические испытания на людях уже в следующем году.
Наночастицы, которые часто изготавливаются из пластмассы или металлов типа серебра, могут также ослаблять бактерии, разрушая их защитные клеточные мембраны или вызывая повреждения ДНК. С наночастицами легко работать, поскольку они сами себя строят. «Вы контролируете температуру, растворитель и все остальное, а эти молекулы самостоятельно собираются в наночастицу», говорит Чжан.
Наночастицы могут быть дороже традиционных антибиотиков. И доставить их в нужное место в организме тоже может быть проблемой. Другая проблема заключается в том, чтобы убедиться, что наночастицы состоят из материалов, которые не будут вызывать немедленный иммунный ответ, и будут разрушаться через время, чтобы не накапливаться в теле.
Остаются вопросы касательно долгосрочной безопасности некоторых из этих вещей, говорит Лу.
Особая доставка
Чтобы сделать существующие антибиотики более эффективными, можно применить альтернативные методы лечения. К примеру, сейчас ученые изучают, как можно было бы использовать наночастицы для доставки противораковых препаратов и антибиотиков.
Антибиотики распространяются по всему телу и являются токсичными в высоких дозах. С помощью наночастиц можно было бы высвобождать концентрированные порции лекарственных препаратов. Тысячи молекул лекарства можно было бы засунуть внутрь одной наночастицы.
«Они легко могут просто крепиться к мембране и постепенно высвобождать лекарственные средства прямо на бактерии», говорит Чжан. Следовательно, более эффективный груз можно было бы более точно направлять, не повышая общую дозу препарата. Таким образом можно было бы подавить механизм устойчивости бактерий — они бы просто не вырабатывали сопротивление против точечно воздействующих антибиотиков.
Проблема наночастиц, как и многих других инструментов, в том, что иммунная система видит в них угрозу. «По размерам они очень похожи на вирусы. Наше тело научится защищаться от этих наночастиц, или вирусов, если вы не защитите их».
Чжан и его коллеги замаскировали наночастицы в пиджачки, сделанные из мембран тромбоцитов — клеток, которые помогают крови сворачиваться. Со стороны наночастицы похожи на эти миниатюрные клетки крови. Некоторые бактерии привлекаются тромбоцитами — с их помощью те маскируются от иммунной системы. Покрытые тромбоцитами наночастицы могли бы сыграть дважды, привлекая захватчиков с тем, чтобы взорвать их лекарственным препаратом.
Все наночастицы будут высвобождать лекарственные препараты в присутствии бактерий, говорит Чжан. С помощью покрытых тромбоцитами частиц он уже вылечил мышей, инфицированных штаммом MRSA, устойчивым ко многим антибиотикам.
Прямая атака
Иногда, впрочем, полумеры не помогают. Существуют альтернативы традиционным антибиотикам, которые могут убивать бактерий. Одна из стратегий — создать искусственные версии антимикробных пептидов (АМП), которые являются частью врожденного иммунного ответа у микробов, растений и животных (вроде тасманийских дьяволов). Эти компоненты атакуют мембрану патогена и сеют хаос внутри клетки.
В рамках недавно проведенного проекта, де ла Фуэнте сотрудничал с Лу и другими, чтобы выбрать нетоксичный АМП, обнаруженный у простых морских животных, называемых оболочниками. Ученые добавили несколько аминокислот к основной настройке, улучшив ее способность лечить мышей, инфицированных устойчивыми к антибиотикам штаммами кишечной палочки или MRSA. Укрепленный АМП также укрепляет иммунную систему грызунов, уменьшает воспаление и призывает помощь в форме белых кровяных клеток.
Антимикробные пептиды могут победить широкий спектр патогенов, и бактерии с трудом вырабатывают устойчивость к ним. «По сравнению с обычными антибиотиками, эти пептиды более эффективны во многих случаях», говорит де ла Фуэнте.
АМП состоят из относительно коротких цепочек аминокислот, строительных блоков белка. Поэтому их довольно просто (хотя и дорого) строить. «Нам еще предстоит снизить стоимость», говорит де ла Фуэнте. Ученые изучают способы создания АМП более дешевым путем программирования микробов, чтобы не полагаться на машину и позволить микробам делать все самостоятельно.
Тем не менее существуют опасения, что АМП может накинуться на клетки носителя. И как со многими альтернативами антибиотиков, отправить пептиды в нужное место в достаточно высокой концентрации, чтобы сохранить эффективность, может быть проблемой. В краткосрочной перспективе более вероятно локальное применение, считает де ла Фуэнте. Эти пептиды можно было бы включить, например, в крем, который можно было бы применить на открытую рану или на место поражения кожи инфекцией. Также их можно было бы использовать для покрытия столов, компьютеров, хирургических инструментов или катетеров, чтобы препятствовать появлению колоний микробов на них.
Ре-сенсибилизация
Еще один способ ослабить бактерии — это избавить их от устойчивости, которую они выработали к антибиотикам. Для таких миссий можно было бы использовать вирусы, которые специализируются на поедании бактерий, бактериофаги.
Бактериофаги — крайне эффективные убийцы бактерий, но благодаря генной инженерии ученые могли бы дать им новые способности, включая и восстановление чувствительности бактерий к традиционным лекарствам.
Перепрограммированные бактериофаги могут зацикливаться на бактериях, несущих гены, придающие устойчивости к антибиотикам, убирать эту способность или убивать бактерий. Когда резистентные микробы будут уничтожены или обезврежены, оставшаяся популяция будет уязвима к антибиотикам.
Другой метод, позволяющий бактериям противостоять антибиотиков, заключается в секретировании соединений, создающих биопленку, через которую не может проникнуть препарат. Можно создать бактериофагов, которые будут проедать биопленку.
В природе бактериофаги могут убивать непосредственно бактерий. Некоторые из них включают свою ДНК в бактерий, и чтобы высвободить себя, просто проедают клеточную стенку, взрывая клетку, говорит Лу. Другие выступают в роли паразитов.
Бактериофаги были обнаружены около сотни лет назад. В США их вытеснили антибиотики, но в России и в некоторых странах Восточной Европы их продолжают использовать. По мере роста антибиотикорезистентных бактерий ученые снова обращаются к бактериофагам — они так же эффективны в лечении людей, просто клинические испытания это пока не подтвердили.
Одно из преимуществ таких вирусов в том, что они могут самовоспроизводиться. Можно поместить лишь небольшое количество и убить множество бактерий. И поскольку им нужны живые клетки для воспроизводства, они перестанут воспроизводиться сразу же, как только будут уничтожены все клетки носителя.
Тем не менее, как и другие альтернативы, бактериофаги могут вызывать ответ иммунной системы. «Если вы введете какой-нибудь вирус или чужеродный пептид в организм человека, всегда есть шанс, что последует реакция», говорит Лу. Другой повод для беспокойства в том, что некоторые фаги могут подхватить гены, связанные с устойчивостью к антибиотикам, и передать их другим бактериям.
Но они вряд ли повредят ткани человека. Бактериофаги не размножаются в человеческих клетках. Внутри нас куча бактериофагов — сложно сказать, что они для нас чужие.
Личный контакт
Некоторые альтернативные методы лечения можно было бы приспособить для борьбы с определенными микробами. Здесь, опять же, бактериофаги являются идеальными кандидатами. «Они по сути естественный враг бактерий», говорит Лу. Обычно, «если вы находите бактерий, вы находите и бактериофагов».
Традиционные антибиотики зачастую убивают бактерий без разбора — в том числе и в естественном микробиоме нашего тела, который играет важную роль для нашего здоровья. Это ковровая бомбардировка, которая убивает всё.
Вирусы предлагают более персонализированный подход. «Можно попытаться сохранить хорошие бактерии и при этом убить вредные», говорит Лу.
Однако эта специфика тоже палка о двух концах. Чтобы охватить достаточное количество различных бактерий, которые могут инфицировать пациента, в коктейле придется замешать множество вирусов. И хотя бактериофагов не очень дорого выращивать, коктейли из множества вирусов — совсем другой вопрос.
Лу работает над созданием коктейлей бактериофагов, построенных на безопасных лесах. Определяя область, которую должны заражать бактериофаги, вы можете атаковать различные бактерии, направлять бактериофагов в разные стороны. Осталось только понять, как это делать.
Как бы то ни было, трудно создавать эффективное лекарство, не зная, что является причиной инфекции. Если вы пойдете к врачу, он не сможет обеспечить вам лечение в узком спектре, если не будет знать, какие бактерии вам досаждают.
Врачам необходимы более быстрые методы диагностики, чтобы они могли выяснять тип целевых бактерий и насколько они устойчивы к традиционным антибиотикам. Лу и его коллеги работают над созданием быстрой и дешевой диагностики. Когда они заражают свои целевые бактерии, они подсвечивают их тем же белком, который используют светлячки. Просто дайте образец бактериофагов пациенту и «сможете понять, светится образец или нет, присутствуют бактерии в нем или нет», говорит Лу.
Широкий арсенал
Это не все оружие, которое мы добавляем в свой арсенал. Ученые изучают другие варианты, вроде отправки других бактерий на борьбу с патогенами, поиска новых антибиотиков, а также использования антител, ну и другого.
«Вряд ли можно полагаться на один метод или одну технологию, чтобы искоренить проблему целиком», говорит Чжан. Изучение супербактерий с разных сторон, совмещение новых тактик и традиционных методов лечения, расширит наш арсенал.
Пройдет несколько лет, прежде чем новые инструменты будут одобрены для широкого использования. И некоторое время альтернативные противомикробные методы будут использоваться лишь тогда, когда антибиотики уже не помогают. Дешевизна и эффективность антибиотиков — основная причина, почему от них трудно отказаться. Но в долгосрочной перспективе это будет единственным вариантом.
Автор: Илья Хель