У стволовых клеток есть способность видоизменяться для замены мёртвых и повреждённых клеток. Но как стволовая клетка решает, в какой вид клеток ей трансформироваться в той или иной ситуации?
Используя кишечные органоиды, учёные идентифицировали новый ген, кодирующий белок Daam1, который, запуская развитие секреторных клеток кишечника, играет чрезвычайно важную роль. Данное открытие выводит онкологические исследования на новый уровень.
У стволовых клеток есть способность видоизменяться для замены мёртвых и повреждённых клеток. Но как стволовая клетка решает, в какой вид клеток ей трансформироваться в той или иной ситуации? Используя кишечные органоиды, научно-исследовательская группа IMBA и Института фундаментальных наук (Institute for Basic Science) под руководством Бон-Гён Ку (Bon-Kyoung Koo) идентифицировала новый ген, кодирующий белок Daam1, который, запуская развитие секреторных клеток кишечника, играет чрезвычайно важную роль. Результаты этого исследования опубликованы в Science Advances. Данное открытие выводит онкологические исследования на новый уровень.
Кое в чём наши тела подобны автомобилям: для длительной эксплуатации их следует регулярно проверять и ремонтировать. Чтобы органы тела продолжали функционировать, все повреждённые или мёртвые клетки нужно заменять. Замена осуществляется благодаря находящимся в тканях стволовым клеткам взрослого человека. Эти клетки, в отличие от эмбриональных стволовых клеток, способных превращаться в любые клетки организма, создают разнообразные клетки только той ткани, к которой принадлежат. Но как тканеспецифичные стволовые клетки узнают, какого вида клетки нужно сформировать? Работавший в IMBA, в лаборатории Бон-Гён Ку, постдокторант Габриэле Колоцца (Gabriele Colozza), ныне директор Центра геномной инженерии Института фундаментальных наук в Южной Корее, решил исследовать этот вопрос, используя стволовые клетки кишечника.
Кишечник — постоянная строительная площадка
«Жизнь клеток в нашем кишечнике экстремальна», — объясняет Колоцца. На них оказывают мощное негативное влияние механические воздействия, пищеварительные ферменты и колебания рН. Чтобы компенсировать наносимый кишечным клеткам урон, стволовые клетки слизистой оболочки кишечника дифференцируются, создавая новые кишечные клетки. «Повреждённые клетки необходимо заменять, но обновление стволовых клеток и превращение их в другие виды клеток представляет собой весьма хрупкое балансирование над пропастью: с одной стороны, неконтролируемая пролиферация стволовых клеток может привести к образованию опухоли, а с другой стороны, если произойдёт дифференциация слишком большого количества стволовых клеток, ткань станет испытывать их дефицит, который грозит ей утратой способности самообновляться».
Тщательная настройка указанного баланса производится сигнальными путями и контурами обратной связи, благодаря которым клетки имеют возможность взаимодействовать друг с другом. Один из важнейших путей — Wnt. Известно, что этот сигнальный путь играет видную роль в эмбриональном развитии, т. е. ему свойственна сверхактивность, и если его не контролировать, он может привести к чрезмерному делению клеток и образованию опухолей.
Идентифицирован молекулярный партнёр
Хорошо известным антагонистом передачи сигналов по пути Wnt является контролирующий Wnt белок Rnf43, который впервые идентифицировал Бон-Гён Ку. Ещё до исследования Колоццы учёные знали, что Rnf43 нацелен на рецептор Wnt Frizzled и помечает его для деградации.
«Мы хотели выяснить, как работает Rnf43, а ещё — что, в свою очередь, контролирует работу Rnf43 и помогает ему регулировать передачу сигналов по пути Wnt».
Как было известно из более ранних исследований, одного Rnf43 недостаточно для разрушения находящегося в плазматической мембране Wnt-рецептора Frizzled.
«В ходе нашего исследования, чтобы выявить белки, которые взаимодействуют с Rnf43, мы проводили биохимический анализ».
Ключевым партнёром Rnf43 оказался белок Daam1.
Чтобы понять, как Daam1 регулирует Rnf43 и влияет на ткани, в которых он действует, Колоцца обратился к кишечным органоидам.
«Без Daam1, как мы установили, Rnf43 не может быть активным, а значит, не может каким бы то ни было образом регулировать передачу сигналов по пути Wnt. Дальнейшая работа с клетками показала, что Daam1 нужен Rnf43 для перемещения Wnt-рецептора Frizzled в везикулы, называемые эндосомами. Из эндосом Frizzled перемещается в лизосомы, где он деградирует, и его деградация затрудняет передачу сигналов по пути Wnt», — добавляет Колоцца.
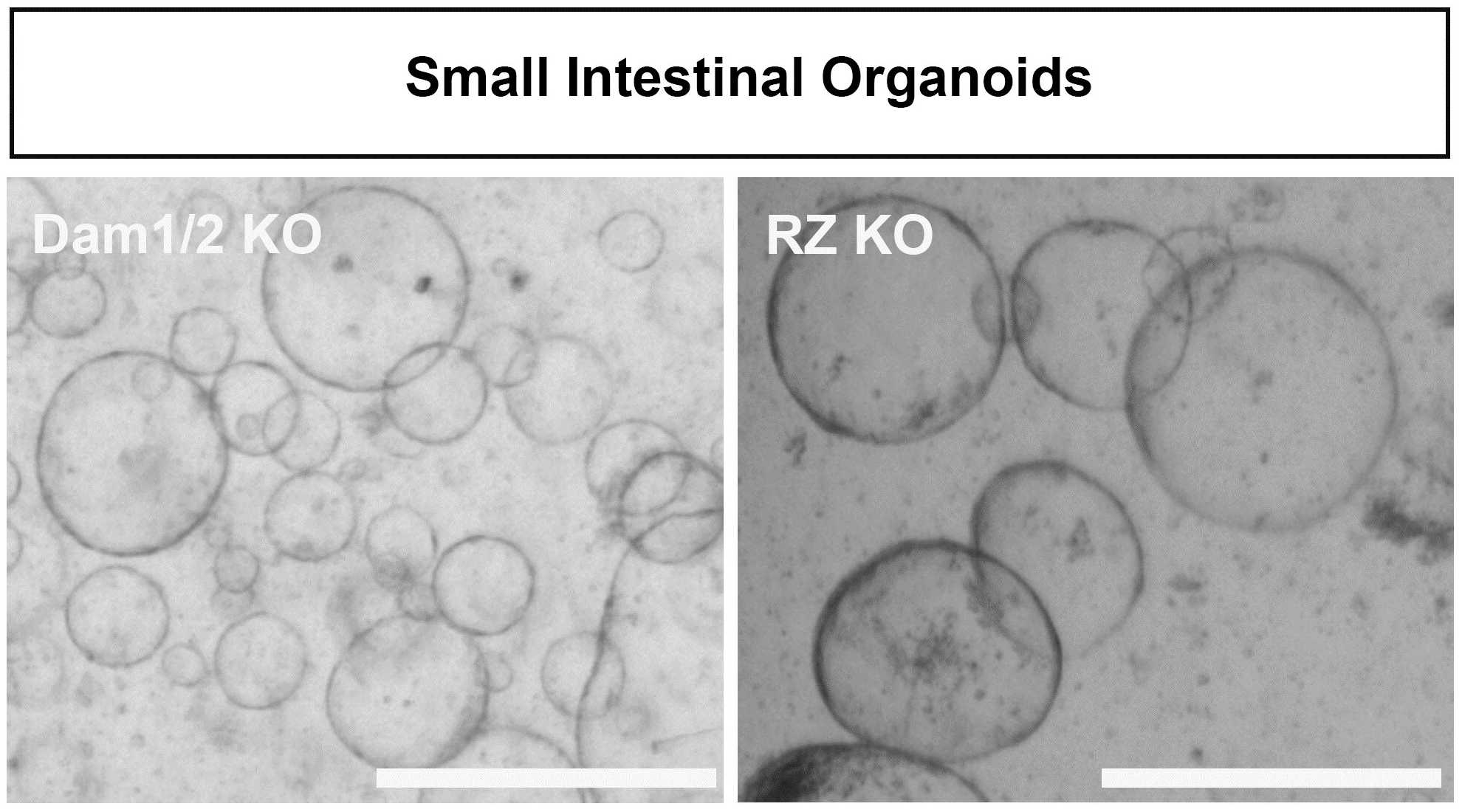
Кишечные органоиды представляют собой трёхмерные клеточные культуры, которые выращиваются из стволовых клеток кишечника взрослого человека для имитации слизистой оболочки кишечника. Органоиды позволили Колоцце выяснить, как Rnf43 и Daam1 влияют на хрупкий баланс обновления и дифференциации стволовых клеток в кишечнике. «Оказалось, что, нокаутируя Rnf43 или Daam1, мы превращаем органоиды в опухолевидные структуры. Эти опухолевидные органоиды продолжают расти даже после удаления обычных для них факторов роста, таких как R-спондин».
Запуск формирования клеток Панета
Проверка полученных данных на мышиных тканях привела команду Колоццы к сюрпризу. «При отсутствии в кишечнике Rnf43 опухоли росли — как и ожидалось. Но при отсутствии Daam1 опухоли не росли. Эта потрясающая разница озадачила нас: как может отсутствие одного из факторов, которые, как показали опыты с органоидами, аналогично влияют на один и тот же путь, привести к столь разным результатам?»
Внимательно изучив кишечник, Колоцца заметил, что в кишечнике без Rnf43 было полно секреторных клеток особого типа — клеток Панета. А вот в кишечнике без Daam1, напротив, повышенного содержания клеток Панета не наблюдалось. Клетки Панета секретируют факторы роста, такие как стимулирующий клеточное деление белок Wnt. «Для эффективного формирования клеток Панета необходим Daam1. При активном Daam1 стволовые клетки дифференцируются с образованием клеток Панета. При пассивном Daam1 стволовые клетки дифференцируются в клетки другого типа».
Чтобы расти, опухоли изменяют свою нишу
Итак, существует связь между молекулярными результатами и клетками Панета. Именно она объясняет озадачившую исследователей разницу между кишечником и органоидами. «О том, чтобы органоидная культура имела факторы роста, заботимся мы, учёные, поэтому нокаут как Rnf43, так и Daam1 приводит к образованию опухолевидных органоидов. Но в кишечнике нет крошечных учёных, которые снабжали бы его факторами роста. Вместо учёных наличие факторов роста, таких как Wnt, обеспечивают клетки Панета. Они-то и создают правильные условия для выживания и деления стволовых клеток. Если клетки Панета в дефиците, — например, когда Daam1 не способствует превращению клеток в клетки Панета, — активного деления стволовых клеток нет. Но если клеток Панета слишком много, — например, в кишечнике без Rnf43, — избыточные факторы роста могут способствовать образованию опухолей».
Исследование Колоццы и его коллег — первое генетическое доказательство того, что Daam1, один из элементов неканонического пути Wnt, важен для спецификации клеток Панета и непосредственно участвует в развитии этих имеющих ключевое значение секреторных клеток. Кроме того, полученные данные проливают дополнительный свет на важную роль ниши стволовых клеток.
«Мы показали, что опухолевые клетки изменяют свою микросреду и влияют на поддерживающую их среду таким образом, чтобы для их роста были более благоприятные условия».
Перевод: Александр Горлов