Исследователям из Израиля удалось первыми в мире создать трехмерную нейронную сеть для регенерации повреждений спинного мозга.
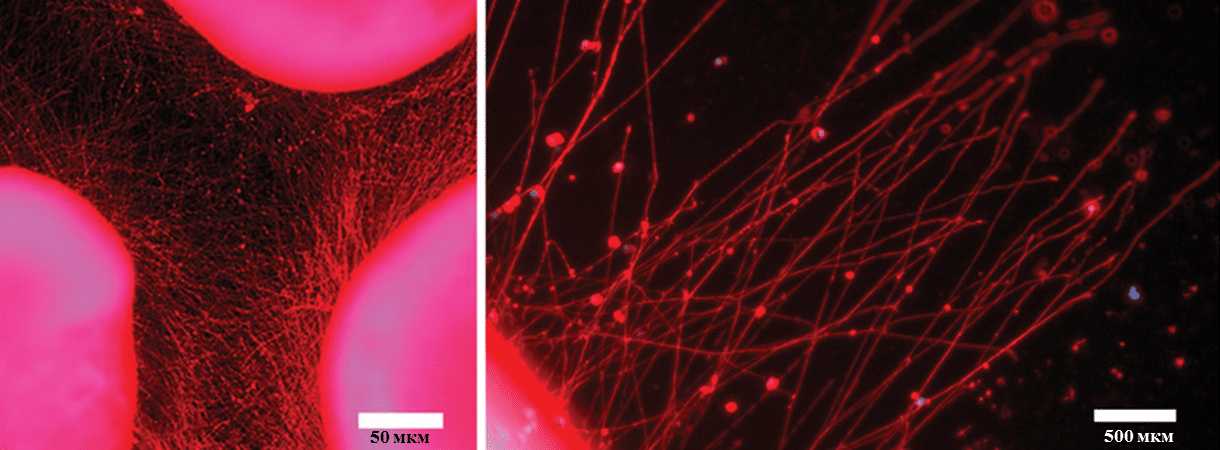
Полученные из стволовых клеток имплантаты позволили восстановить морфологию и функции спинного мозга мышей, тем самым вернув им способность ходить. Авторы рассчитывают выйти на стадию клинических испытаний на людях в течение следующих нескольких лет.
Травматическое повреждение спинного мозга (ТПСН) — поражение любой части спинного мозга или нервов позвоночного канала в результате травмы, аварии, болезни или дегенерации (например, рака). В зависимости от тяжести травмы ТПСН может привести к частичному или полному нарушению работы систем регуляции органов, потере чувствительности и двигательных функций конечностей и частей тела, находящихся ниже уровня повреждения. Ежегодно в мире от 250 до 500 тысяч человек получают повреждения спинного мозга.
Ранее предлагались самые разные способы восстановления поврежденного спинного мозга, включая трансплантацию различных типов клеток или биоматериалов в место повреждения в острой фазе (то есть в первые сутки после ТПСН). Однако все эти попытки были безуспешными, в основном из-за двух факторов: во-первых, иммунного ответа на чужеродные клетки, в результате которого происходит отторжение трансплантата; во-вторых, имплантации клеток, не организованных в функциональную сеть и поэтому не способных выполнять необходимые функции.
Исследователям из Центра регенеративной биотехнологии Сагол при Тель-Авивском университете (Израиль) удалось решить обе проблемы. Чтобы преодолеть риск отторжения, предлагается использовать индуцированные плюрипотентные стволовые клетки (ИПСК) самого пациента. Значит, у него будут брать образец обычных соматических клеток (например, в описываемой работе — из жировой ткани живота) и при помощи генной инженерии перепрограммировать в стволовые клетки, которые затем превратят в нейроны спинного мозга.
Для решения второй проблемы — формирования правильной функциональной сети — исследователи разработали методику создания специального персонализированного гидрогеля на основе все того же образца, взятого из жировой ткани. Созданный таким образом гидрогель не вызывает отторжения при трансплантации и вдобавок образует идеальную среду для формирования трехмерной нейронной сети, содержащей двигательные нейроны.
В результате созданные таким образом имплантаты человеческого спинного мозга имплантировали в лабораторные модели (мыши), разделенные на две группы: недавно парализованных (острая модель ТПСМ) и парализованных в течение длительного времени, что эквивалентно году в человеческом исчислении (хроническая модель ТПСМ). После имплантации 100% лабораторных моделей с острым параличом и 80% моделей с хроническим параличом восстановили способность ходить.
Профессор Тал Двир (Tal Dvir), ведущий автор исследования, поясняет: «Животные-модели прошли быстрый процесс реабилитации, в конце которого они могли довольно хорошо ходить. Это первый в мире случай, когда имплантированные ткани человека, полученные методом клеточной инженерии, способствовали восстановлению модели животного с длительным хроническим параличом, которая служит наиболее подходящей моделью лечения паралича у людей».
Авторы работы надеются выйти на стадию клинических испытаний на людях в течение следующих нескольких лет. Доклиническая программа уже обсуждалась с FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США).
«Поскольку мы предлагаем передовую технологию регенеративной медицины и поскольку на сегодня нет альтернативы для парализованных пациентов, у нас есть все основания ожидать относительно быстрого одобрения нашей технологии», — подытожил профессор Двир.
Статья с результатами исследования опубликована в журнале Advanced Science.
Автор: Даниил Сухинов