Немецкие ученые разработали опиоид, который действует только в месте воспаления, не вызывая общих побочных эффектов. Результаты работы опубликованы в журнале Science.
Опиоиды обладают наиболее мощным обезболивающим действием из всех имеющихся анальгетиков. Фактически это единственные препараты, способные купировать сильную боль, например, при тяжелых травмах, инфаркте миокарда, нейропатической боли, онкологических и других заболеваниях.
Однако их применение сопряжено с нежелательными побочными эффектами, такими как угнетение дыхания, запоры, чрезмерная сонливость, тошнота, кожный зуд, а также риск формирования привыкания и зависимости. Поэтому многочисленные научные коллективы занимаются поиском эффективных и безопасных альтернатив этим лекарствам. Как правило, речь идет о препаратах центрального действия, то есть действующих на антиноцицептивную (препятствующую восприятию боли) систему мозга, как и опиоиды. Однако при некоторых болезненных состояниях, таких как травмы, операции, артриты и другие, было бы достаточно местного действия анальгетиков.
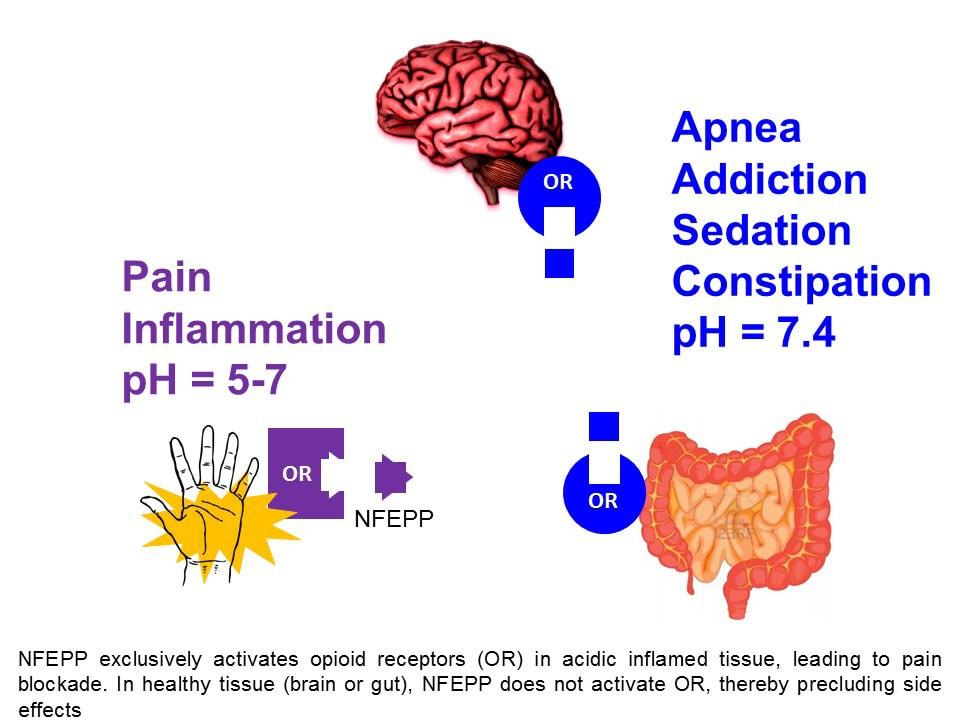
В поиске подобного препарата сотрудники Свободного университета Берлина и Университета имени Цузе оттолкнулись от того факта, что общим признаком воспаленной (поврежденной) ткани является ее ацидоз, или кислая среда, в то время как у здоровых тканей среда слабощелочная. Ацидоз при воспалении повышает активацию периферических опиоидных мю-рецепторов за счет усиленного функционирования их G-белков, передающих сигнал внутрь клетки, и протонирования лигандов (эндо- и экзогенных опиоидов), необходимого для связывания их с рецептором. В таких условиях именно периферические рецепторы в наибольшей степени отвечают за обезболивание. Таким образом, опиоиды, которые активируются только в кислой среде, теоретически могли бы обеспечить адекватную аналгезию в месте повреждения без действия на весь организм.
Сильный агонист опиоидных рецепторов фентанил способен активировать их как в физиологической, так и в кислой среде. Ученые провели компьютерную симуляцию связывания в обеих этих средах с мю-рецепторами различных фторзамещенных производных фентанила, поскольку фтор притягивает протоны, смещая диссоциацию (в этом контексте — активацию) всей молекулы в кислую сторону.
По итогам симуляции было выбрано и синтезировано фторзамещенное производное фентанила NFEPP (N-(3-фтор-1-фенэтилпиперидин-4-ил)-N-фенилпропионамид). Эксперименты с культурами клеток подтвердили, что он связывается с мю-рецепторами и активирует их G-белок в кислой среде значительно сильнее, чем в нейтральной и щелочной.
На следующем этапе экспериментов ученые вводили фентанил и NFEPP крысам с моделями острого и хронического воспаления и травмой. Оба вещества производили адекватное обезболивание, однако, в отличие от общего действия фентанила, NFEPP вызывал аналгезию только в поврежденных тканях. Совместное введение препаратов с антагонистом периферических опиоидных рецепторов NLXM (налоксона метйодидом), не проникающим в мозг, подтвердило, что NFEPP действует только за счет этих рецепторов.
Кроме того, NFEPP в дозах, в 2,5 раза превышающих максимальные для фентанила, не вызывал у животных таких побочных эффектов как самовведение (показатель пристрастия к действию вещества), уменьшение подвижности и запор, а также не влиял на частоту дыхания и сердечных сокращений.
«Выбор в качестве мишени патологических, а не физиологических конформаций рецепторов и лигандов представляет собой смену парадигмы дизайна лекарств. Таким способом был получен новый опиоидный анальгетик с аналогичной обычному фентанилу эффективностью, избавленный от вредных побочных эффектов», — пишут авторы работы.
В начале 2016 года фармакологи из Университета Тулейн в Новом Орлеане сообщили о создании четырех опиоидов центрального действия без основных побочных эффектов. Они представляют собой пептиды, полученные модификацией природных нейромедиаторов эндоморфинов. По мнению исследователей, небольшая выраженность побочных эффектов связана с тем, что они, в отличие от морфина, не действуют на рецепторы нейроглии (вспомогательных клеток нервной системы). В августе того же года международная группа ученых представила низкомолекулярный опиоид, также избавленный от основных недостатков препаратов этой группы. В отличие от них он активирует только «классический» внутриклеточный сигнальный путь, связанный с G-белком и отвечающий за аналгезию, но не альтернативный бета-аррестиновый, через который реализуются нежелательные эффекты.
Автор: Олег Лищук